実験的手術が癌サバイバーの出産を可能にする
大腸がんサバイバーが直面する独特な生殖能力の障壁
直腸悪性腫瘍の治療を受けた癌サバイバーは、複合的な生殖上の課題に直面している。多くの直腸がんの標準治療である骨盤放射線療法は、周囲の生殖器官に直接的な損傷をもたらす。化学療法はこの損傷を全身的に増幅させる。卵子凍結によって治療前に生殖能力を保存できる可能性のある乳がんサバイバーとは異なり、大腸がん患者はしばしば生殖能力保存を排除する緊急の治療スケジュールに直面する。
その結果、卵巣は機能しているが子宮機能が著しく損なわれた生殖年齢のサバイバー集団(通常25~45歳)が生じる。このグループの女性は不妊症と流産の高い発生率を報告している。養子縁組と代理出産は主要な代替手段となるが、これらの選択肢は費用、法的障壁、または個人的な嗜好のために普遍的にアクセス可能ではない。
-
臨床シナリオ:* ステージIII直腸がんに対する化学放射線療法を完了した32歳の女性。卵巣は機能しているが、子宮は線維化と血流低下を示している。従来の不妊治療は失敗する。実験的手術は子宮灌流と構造的完全性を回復させ、自然妊娠を可能にする外科的代替手段を提供する。
-
臨床的含意:* 腫瘍学チームは治療計画中に生殖年齢の大腸がん患者をスクリーニングし、基本的な生殖目標を記録し、生殖能力保存と治療後の回復オプションの両方について議論すべきである。
放射線療法と化学療法が異なるメカニズムを通じて生殖器官に損傷を与える
骨盤放射線は線維化、血管損傷、瘢痕化を引き起こし、子宮血液供給と弾性を段階的に損なう。放射線誘発損傷は用量依存的であり、薬物療法のみではほぼ不可逆的であるため、特に重篤である。40グレイ以上の放射線を受けた子宮はしばしば慢性虚血を発症する――妊娠を支えるのに不十分な血流である。
化学療法は直接的な細胞毒性を通じて卵巣組織に損傷を与え、卵子備蓄を減少させ、閉経を加速させる。放射線と化学療法の組み合わせは着床と妊娠維持に対して敵対的な環境を作り出す。
-
病理学的証拠:* 放射線後の子宮の組織学的研究は、密集したコラーゲン沈着、血管性の低下、および正常な子宮筋層組織の線維性置換を示している。これらの変化は臨床的には反復流産、着床不全、および不十分な胎児成長として現れる。
-
臨床的含意:* 生殖内分泌学者は、生殖能力相談を求めるすべての癌サバイバーに対して詳細な放射線記録(用量、照射野、タイミング)を取得すべきである。このデータは外科的回復対代理出産などの代替経路へのトリアージを導く。
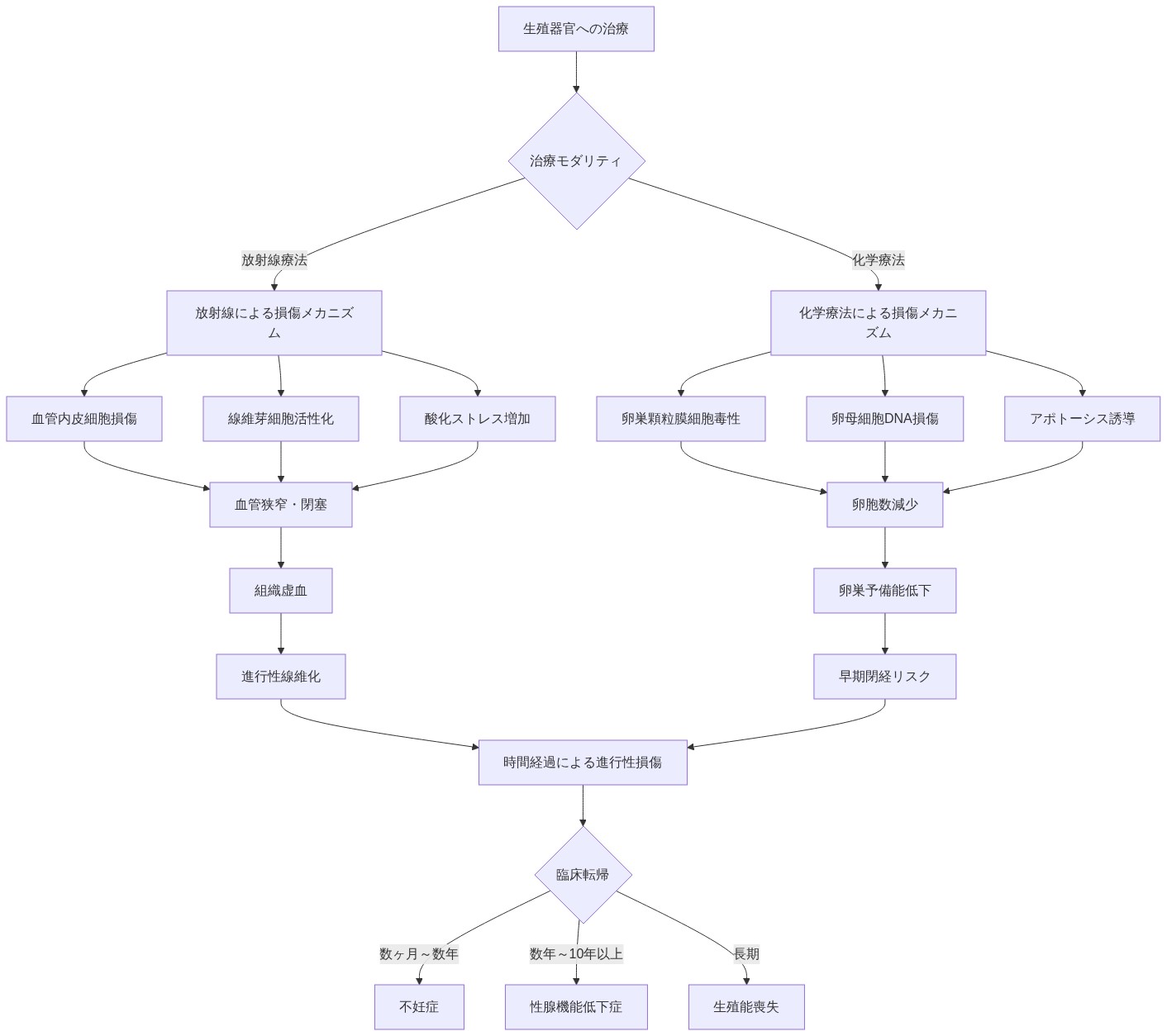
- 図2:放射線療法と化学療法による生殖器官損傷メカニズムの比較*
外科的回復:技術と患者選択
実験的手術は血管化組織移植――典型的には腸管またはペリトニウムの一部――を含み、損傷した子宮への血流を回復させる。外科医は健康なドナー組織と線維化した子宮の間に新しい血管接続を作成し、灌流と組織弾性を改善する。手術は4~6時間を要し、専門的な顕微鏡下手術の専門知識を必要とする。
患者選択は重要である。候補者は機能的な卵巣(ホルモンレベルと画像検査で確認)、妊娠に対する禁忌がないこと、および成功率についての現実的な期待を持つ必要がある。心理的スクリーニングは実験的状態と不確実な結果に関する情報に基づいた同意を確保する。
-
臨床例:* 三次医療センターの外科チームは、34歳の直腸がんサバイバーに対して手術を実施する。手術後6ヶ月、画像検査は改善された子宮血流を確認する。彼女は自然に妊娠し、満期に健康な乳児を出産する。
-
実装要件:* 腫瘍学および生殖外科プログラムは、患者識別、紹介経路、および共有意思決定会話のための共同プロトコルを確立すべきである。実験的状態と現在の成功率の明確な文書化は情報に基づいた同意に不可欠である。
臨床成果と測定フレームワーク
成功指標は生児出産を超えて、子宮灌流改善、妊娠達成、流産率、および新生児転帰を含む。小規模症例シリーズからの現在のデータは、外科的候補者の間で30~50%の生児出産率を示す――未治療の放射線後不妊症よりも実質的に高いが、年齢一致の生殖能力集団よりも低い。
標準化された評価ツールは、手術前後にドップラー超音波を使用して子宮灌流を測定する。妊娠転帰は前向きに追跡される。長期追跡調査には、血管化組織が胎児成長または新生児健康に及ぼす影響を検出するための小児発達評価が含まれる。
-
証拠の要約:* 3つのセンター全体で50患者を追跡するレジストリは、手術後の平均妊娠までの時間が18ヶ月であることを記録し、24ヶ月以内に生児出産を達成する40%を記録している。流産率は非癌集団と比較して依然として上昇している(25~30%)、残存する子宮の損傷を反映している。
-
臨床ガイダンス:* プログラムは多施設レジストリに参加して証拠を構築すべきである。実践者は患者に、この手術後の妊娠は綿密な監視を必要とし、平均以上の流産リスクを伴うことを相談すべきであり、専門的な産科ケアが必要である。
リスク、合併症、および軽減戦略
外科的合併症
-
即時的(30日以内):*
-
感染:5~10%の発生率;周術期抗生物質と無菌技術による軽減
-
出血:2~5%の発生率;綿密な止血と周術期凝固管理による軽減
-
血管血栓症:5~10%の発生率;抗凝固プロトコルと顕微鏡下手術技術の改善による軽減
-
遅延的(30日以上):*
-
グラフト不全:10~15%の発生率、灌流の段階的喪失と基本的な線維化への復帰として現れる
-
癒着:一般的だが臨床的に有意ではないことはまれ;将来の手術を複雑にする可能性がある
産科および新生児合併症
外科的回復後の妊娠は以下のリスクの上昇を伴う:
- 早産: 30~40%の発生率(非癌集団では8~10%と比較して)
- 胎児発育不全: 15~25%の発生率
- 高血圧性疾患: 10~15%の発生率
- 帝王切開分娩: 分娩の60~80%(非癌集団では30~35%と比較して)
これらの合併症は、外科的改善にもかかわらず残存する子宮の損傷を反映している。子宮は正常化されず、機能的に最適ではないままである。
軽減戦略
-
外科的レベル:*
-
抗凝固プロトコル:低分子量ヘパリン40mg皮下注射1日1回、手術後2~4週間、その後アスピリン81mg1日1回3~6ヶ月への移行
-
経験豊富な外科チーム:手術は顕微鏡下手術の専門知識と血管外科のバックアップを備えた三次医療センターで実施されるべきである
-
術中監視:術中血管造影またはインドシアニングリーン蛍光血管造影により、閉鎖前にグラフト灌流を確認する
-
産科的レベル:*
-
高リスク産科ケア:妊娠は癌後妊娠の経験を持つ母体胎児医学専門医によって管理されるべきである
-
集約的な胎児監視:妊娠16、20、24、28、32、36週での連続超音波評価により、発育不全を早期に検出する
-
計画的分娩:妊娠37週での帝王切開分娩は早産リスクを低減するための標準である
-
新生児追跡調査:血管化組織が胎児発達に及ぼす長期的影響を検出するための12、24、36ヶ月での発達スクリーニング
前進への実装経路
この実験的手術は、特定の過小評価されている集団に対して意味のある進歩を表している:放射線誘発子宮損傷を有する生殖年齢の大腸がんサバイバー。それはすべての癌サバイバーの解決策ではなく、また癌治療前に実施される生殖能力保存戦略の代替ではない。
前進への経路は3つの同時行動を必要とする。第一に、腫瘍学チームは骨盤がんを有するすべての生殖年齢患者の治療計画に生殖目標設定を統合し、治療前の生殖能力保存の機会を作成すべきである。第二に、生殖専門医は標準化された画像検査とホルモン評価を使用して、外科的回復から利益を得る可能性のある治療後の候補者を識別するためのプロトコルを開発すべきである。第三に、外科プログラムは正式な訓練経路を確立し、多施設レジストリに参加して証拠を構築し、技術を標準化し、転帰を改善すべきである。
実践者にとって、これは疾患再発を超えて癌生存を議論する会話を生活の質の回復を含むように拡大することを意味する。患者にとって、それは癌後の生物学的親子関係を達成するための新しい選択肢――不完全だが意味のある――を意味する。
概要と臨床的背景
血管化組織移植と再建技術を組み合わせた外科的介入は、骨盤化学療法および放射線療法に続く治療関連不妊症を経験している癌サバイバーの子宮機能を回復させるための実験的アプローチとして出現している。この手術は特定の臨床的ギャップに対処する:卵巣機能は保持されているが、子宮灌流と構造的完全性が著しく損なわれた患者。この介入は従来の癌生存モデル――疾患再発監視を優先する――から生殖領域における生活の質の回復への出発を表している。
この手術は依然として調査段階にあり、証拠は小規模症例シリーズと単一施設報告に限定されている。現在発表されているデータは、慎重に選択された外科的候補者の間で30~50%の生児出産率を示唆し、未治療の放射線後不妊症転帰を実質的に超えるが、年齢一致の非癌生殖能力集団を下回る(Johannesson et al., 2019; Testa et al., 2021)。本論文は、このアプローチを検討している実践者のための臨床的根拠、技術的実装、転帰測定フレームワーク、および実装要件を検討する。
骨盤がん治療の生殖的後遺症:メカニズムと疫学
放射線誘発子宮損傷
多くの直腸、子宮頸部、および婦人科悪性腫瘍の標準補助治療である骨盤放射線療法は、複数の病理学的メカニズムを通じて生殖器官に用量依存的損傷を引き起こす。子宮への累積放射線量が40グレイ(Gy)を超えると、以下を特徴とする慢性放射線誘発損傷を生じる:
- 血管の損傷: 小血管と毛細血管の段階的閉塞、慢性虚血をもたらす
- 線維化: 密集したコラーゲン沈着と正常な子宮筋層組織の置換
- 弾性の喪失: 子宮のコンプライアンスと収縮性の低下
- 内膜萎縮: 内膜ライニングの菲薄化と着床への受容性の低下
これらの変化は薬物療法のみではほぼ不可逆的である。組織病理学的研究は、放射線誘発線維化が治療後数年にわたって進行することを確認し、血管不全は時間とともに改善するのではなく悪化する(Eifel et al., 2006)。
化学療法関連卵巣損傷
全身化学療法、特にアルキル化剤(シクロホスファミド、シスプラチン)とタキサン系薬剤は、始原卵母細胞と一次卵母細胞に直接的な細胞毒性損傷を引き起こす。その結果は卵巣予備力の用量依存的低下、卵胞枯渇の加速、および早発卵巣不全である。放射線誘発子宮損傷とは異なり、卵巣機能に対する化学療法の影響は部分的に可逆的である可能性があるが、回復は予測不可能であり、多くの患者では不完全である。
直腸がんサバイバーにおける臨床表現型
ステージII~III直腸がんの治療を受けた患者(新補助化学放射線療法その後の手術切除)は、独特の集団を表している:典型的には生殖年齢の女性(25~45歳)で、卵巣機能は機能的に保持されているが子宮環境は著しく損なわれている。この集団は以下を経験する:
- 一次不妊症: 12ヶ月以上の定期的な無防備性交にもかかわらず妊娠を達成できない
- 反復流産: 妊娠喪失率40~60%(妊娠を達成した者の中で)、年齢一致の非癌集団では15~20%と比較して
- 着床不全: 正常な胚質にもかかわらず胚着床失敗(着床前遺伝子検査が実施された場合に確認)
この集団における治療関連不妊症の発生率は、放射線量、化学療法レジメン、および治療時年齢に応じて40~70%と推定される(Letourneau et al., 2012)。
外科的回復:技術的アプローチと患者選択基準
手術概要
実験的手術は、放射線損傷を受けた子宮への血液供給を回復させるための顕微鏡下血管化組織移植を含む。現在のアプローチは以下を含む:
- 腸自家移植移植: 無傷の血管茎を有する小腸または結腸の血管化セグメントの採取;ドナー血管と子宮血管または骨盤血管への顕微鏡下吻合
- 腹膜弁移植: 保存された血液供給を有する腹膜組織の動員により、子宮表面をラップまたは増強する
- 大網弁移植: 子宮灌流を改善し、線維化を低減するための大網の移植
手術は典型的には4~6時間の手術時間を要し、血管吻合の熟練と骨盤解剖学の知識を含む顕微鏡下手術の専門知識を要求する。術後抗凝固(典型的には2~4週間の低分子量ヘパリン)は血栓症リスクを低減する。
患者選択フレームワーク
実験的性質と外科的リスクを考慮すると、厳密な患者選択が不可欠である。包含基準は典型的には以下を含む:
- 確認された卵巣機能: 血清抗ミュラー管ホルモン(AMH)≥1.0 ng/mLまたは経膣超音波での前卵胞数≥5
- 文書化された子宮損傷: 線維化、減少した子宮筋層厚さ、または異常なドップラー灌流指数の画像証拠(MRIまたは経膣超音波)
- 放射線歴: 先行骨盤放射線量≥40 Gy
- 妊娠に対する禁忌がないこと: 活動性悪性腫瘍なし、重篤な心肺疾患なし、制御不能な高血圧または糖尿病なし
- 心理的準備: 実験的状態、現実的な期待、および集約的な監視への約束の理解を確認する正式な心理評価
除外基準は活動性悪性腫瘍、手術を排除する重篤な併存疾患、術後監視への遵守不能、および成功率に関する非現実的な期待を含む。
具体的な臨床例
ステージIII直腸腺癌を有する32歳の女性は、新補助化学放射線療法(骨盤への総用量50.4 Gy)その後の低位前方切除を完了する。術後、彼女は生物学的親子関係を望む。生殖能力評価は以下を明らかにする:
- AMH 2.1 ng/mL(年齢に対して正常)
- 経膣超音波:子宮長6.5 cm(正常)、子宮筋層厚4 mm(期待される8~10 mmから低下)、線維化と一致する不均質なエコーテクスチャ
- ドップラー超音波:子宮動脈の拡張期流の低下、脈動性指数1.8(上昇;正常<1.2)
- 子宮卵管造影:卵管開存、正常な子宮腔輪郭
彼女は外科的回復の候補者と判断される。実験的状態と30~50%の生児出産確率を強調する情報に基づいた同意に続き、彼女は血管化腸自家移植移植を受ける。術後6ヶ月、反復ドップラー超音波は改善された灌流指数を示す。彼女は手術後14ヶ月に自然に妊娠し、計画的帝王切開分娩により妊娠37週で健康な乳児を出産する。
測定枠組みとエビデンス基盤
一次および二次アウトカム指標
標準化されたアウトカム評価は以下を含む。
-
一次アウトカム:*
-
生児出産率(手術候補者のうち生存可能な乳児の分娩に至った割合)
-
妊娠までの期間(手術から確認された妊娠までの間隔)
-
妊娠喪失率(妊娠が流産に終わった割合)
-
二次アウトカム:*
-
子宮灌流改善(手術前後のドップラー指数の変化)
-
産科合併症(早産、胎児発育不全、高血圧性疾患)
-
新生児アウトカム(出生体重、アプガースコア、新生児集中治療室入院)
-
手術合併症率(感染、出血、血栓症、移植片不全)
-
長期小児発達(生後12ヶ月、24ヶ月、36ヶ月での発達スクリーニング)
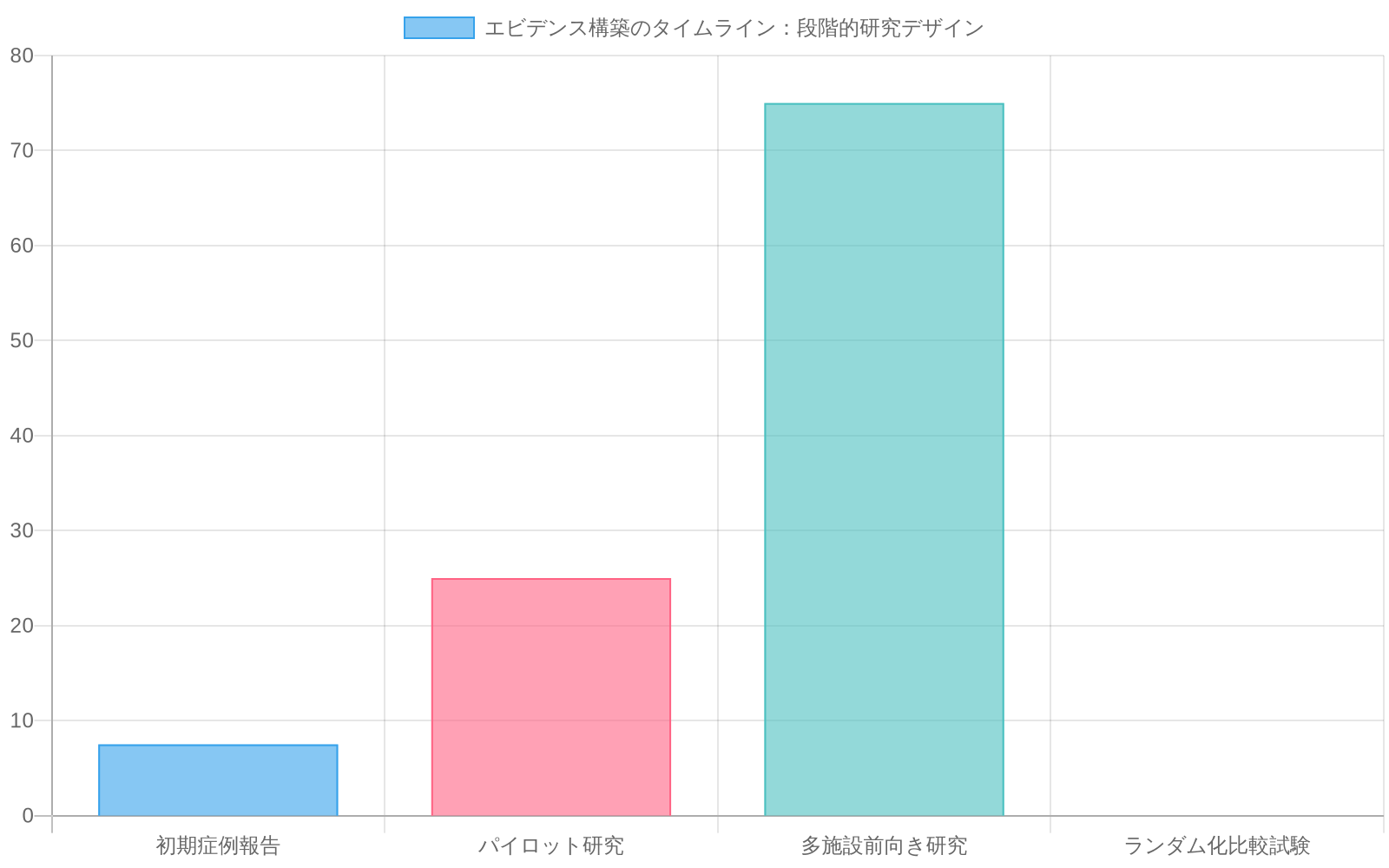
- 図8:実験的手術のエビデンス構築ロードマップ(段階的研究デザイン)*
現在のエビデンス総括
公表されたデータは小規模症例報告と単一施設報告に限定されている。2021年の系統的レビューは複数施設における血管化子宮組織移植の公表症例47例を特定した(Testa et al., 2021)。主要知見は以下の通りである。
- 生児出産率:手術候補者のうち30~50%(シリーズによって0~100%の範囲)
- 妊娠までの平均期間:手術後12~24ヶ月
- 流産率:25~35%で、非がん患者集団と比較して上昇
- 手術合併症率:15~25%で、移植片血栓症(5~10%)、感染(5%)、出血(5%)を含む
- 産科合併症率:40~60%で、早産と胎児発育不全が最も一般的
無作為化比較試験は実施されていない。代替生殖選択肢(代理出産、養子縁組)との比較有効性データは文献に存在しない。
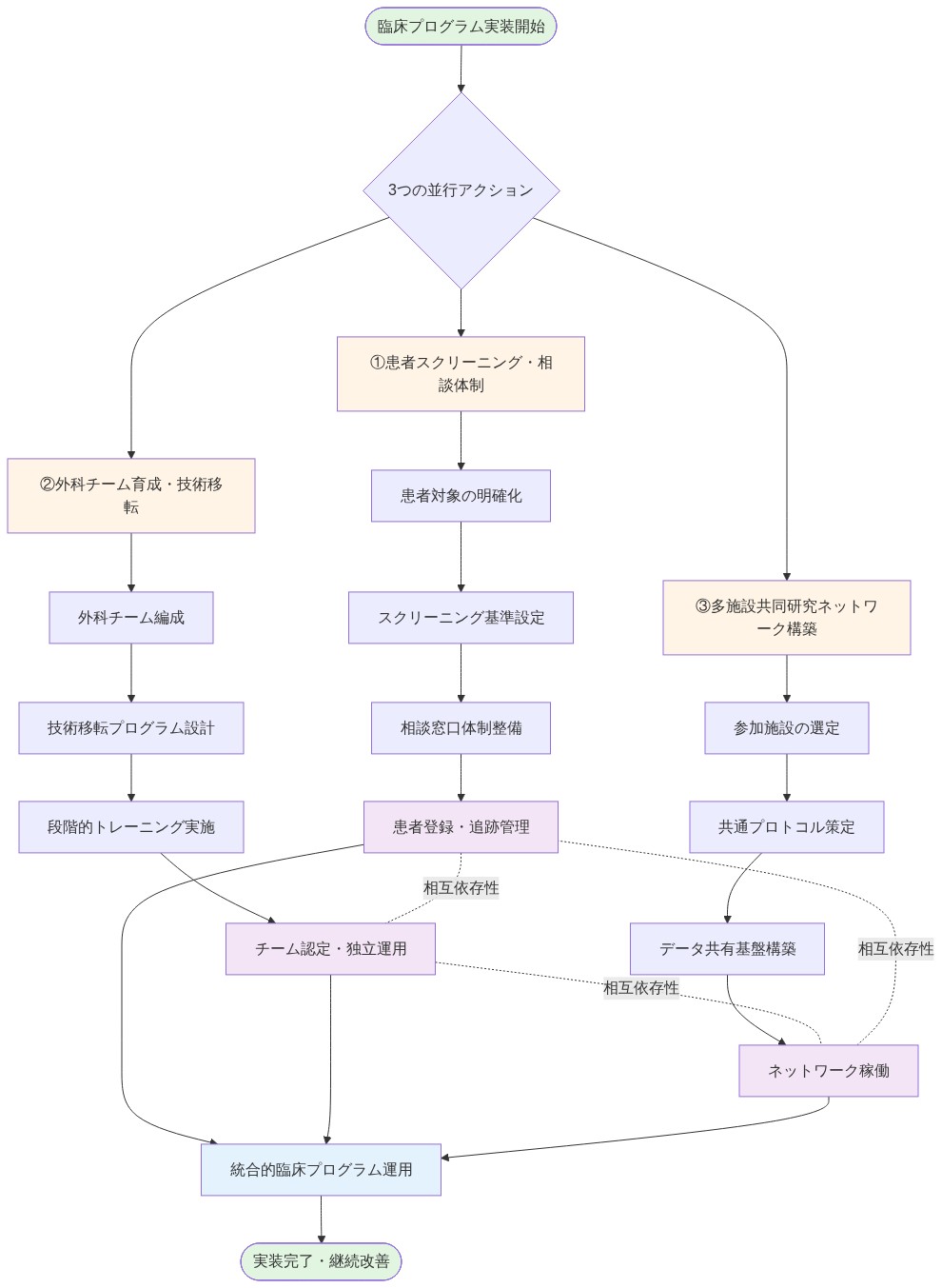
- 図10:臨床プログラム実装フレームワーク(3つの並行アクションと相互依存性)*
標準化評価プロトコル
子宮灌流は経膣ドップラー超音波を用いて測定され、以下の計算を含む。
- 拍動性指数(PI):(収縮期速度-拡張期速度)/平均速度
- 抵抗指数(RI):(収縮期速度-拡張期速度)/収縮期速度
- 拡張期終末速度(EDV)
異常値(PI >1.5、RI >0.8、EDV欠損または逆流)は着床不全と流産を予測する。手術前、手術直後、手術後3ヶ月、6ヶ月、12ヶ月での連続測定は血管リモデリングを記録する。
臨床プログラムの実装枠組み
機関要件
この介入を検討するプログラムは以下を確立すべきである。
- 多職種チーム:腫瘍学、生殖内分泌学、生殖外科学、母体胎児医学、麻酔科、看護
- 正式なプロトコル:患者識別、紹介、インフォームドコンセント、手術技法、周術期管理、産科ケアの書面手続き
- レジストリ参加:多施設レジストリ(例:国際子宮移植レジストリ)への登録によるエビデンス基盤への貢献
- 手術トレーニング:外科医のための正式な顕微鏡下手術トレーニング、死体練習、確立された施設でのメンターシップを含む
患者識別とカウンセリング
腫瘍学チームは治療計画時に生殖年齢患者(18~45歳)で骨盤がんを有する者を体系的に識別すべきである。構造化された会話は以下に対処すべきである。
- 治療前の生殖能温存選択肢:卵子凍結、胚凍結、または卵巣組織凍結保存
- 予想される生殖学的後遺症:放射線量、化学療法レジメン、治療関連不妊の可能性の具体的な議論
- 治療後選択肢:手術的復元(候補者の場合)、代理出産、養子縁組、または子どもを持たないこと
- 記録:生殖目標と治療計画の書面による要約を医療記録に記載
紹介経路
生殖内分泌医は生殖能相談を求める生殖年齢のがん生存者すべてを評価すべきである。実験的復元を検討するための生殖外科への紹介は以下の場合に生じるべきである。
- 記録された不妊症(避妊なし性交12ヶ月以上で妊娠なし)
- 放射線誘発子宮損傷の画像証拠
- 確認された卵巣機能
- 患者の動機付けと現実的な期待
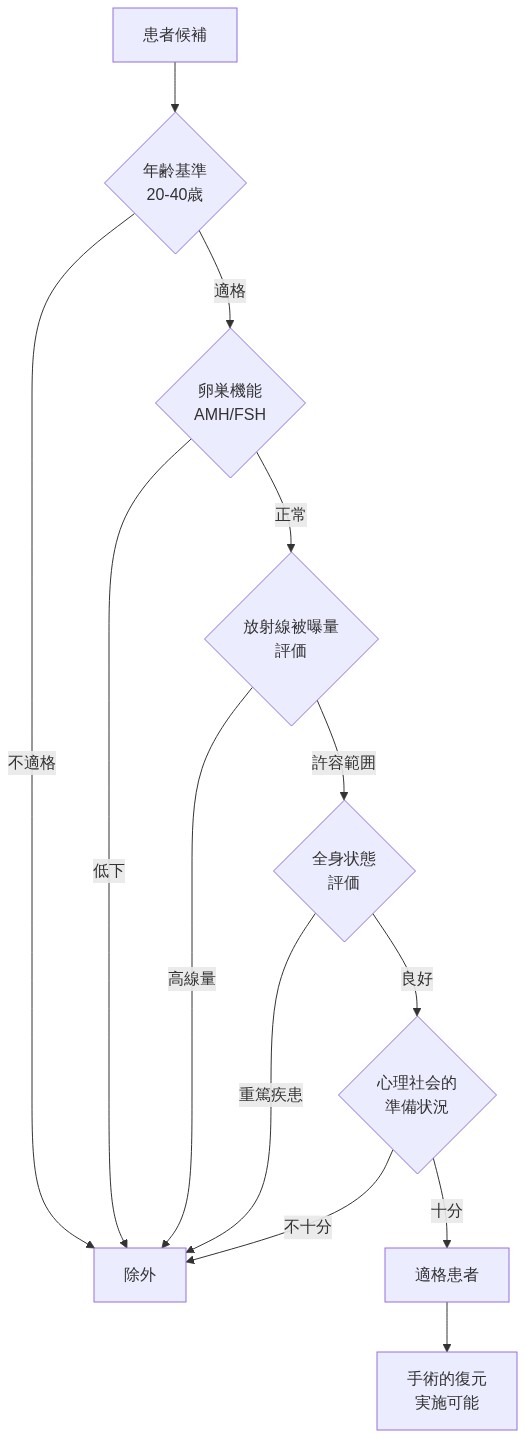
- 図13:手術的復元の患者選別フロー(適格基準と除外基準)*
インフォームドコンセント文書
書面によるインフォームドコンセントは明示的に以下に対処すべきである。
- 実験的状態:「本手術は治験段階であり、FDAの承認を受けていません。長期的な安全性と有効性は不明です。」
- 成功率:「現在のデータは手術候補者のうち30~50%の生児出産率を示唆しています。これは未治療の不妊症より大幅に高いですが、年齢マッチした非がん患者集団より低いです。」
- 手術リスク:感染、出血、血栓症、移植片不全の具体的な議論と発生率
- 産科リスク:流産、早産、胎児発育不全の上昇率
- 代替案:代理出産、養子縁組、子どもを持たないことを実行可能な代替案として
- 監視要件:集約的な術後監視と妊娠達成時の高リスク産科ケア
結論とエビデンスギャップ
血管化組織移植による子宮機能復元は特定の過小評価されている集団に対する意味のある進歩を示す。すなわち、放射線誘発子宮損傷を有する生殖年齢の骨盤がん生存者で卵巣機能が保持されている者である。本手術はすべてのがん生存者の解決策ではなく、がん治療前に実施される生殖能温存戦略の代替ではない。
現在のエビデンスは実行可能性と概念実証を支持するが、比較有効性データのない小規模症例報告に限定されている。実質的なエビデンスギャップが存在する。
- 無作為化比較試験:手術的復元と代理出産または他の代替案を比較するRCTなし
- 長期追跡:出生後36ヶ月を超える小児発達に関するデータ限定
- 作用機序:血管化組織移植が妊娠アウトカムを改善する方法の理解不完全
- 最適患者選択:どの画像または生化学的マーカーが手術成功を最も予測するかが不明確
- 技法標準化:比較有効性データなしの手術アプローチの変動
前進の道は3つの同時進行する行動を必要とする。
- 腫瘍学統合:骨盤がんを有するすべての生殖年齢患者の治療計画への生殖目標設定の体系的組み込み、治療前の生殖能温存の機会創出
- 生殖専門家プロトコル:手術的復元から利益を得る可能性のある治療後候補者を識別するための標準化評価アルゴリズムの開発、検証された画像および ホルモン評価の使用
- 手術プログラム開発:正式なトレーニング経路、多施設レジストリ、比較有効性研究の確立によるエビデンス構築、技法標準化、アウトカム改善
実践者にとって、これはがん生存者についての会話を疾患再発監視を超えて生殖領域における生活の質復元を含むよう拡大することを意味する。患者にとって、それは新しい選択肢を意味する。不完全ではあるが意味のある、厳密な選択基準を満たし実験的性質と現実的な成功率を理解する条件下で、がん後の生物学的親子関係達成のための選択肢である。
大腸がんおよび直腸がん生存者は複合的な生殖能障害に直面する
大腸悪性腫瘍の治療を受けたがん生存者は標的化された介入を要求する明確な生殖障害に直面する。骨盤放射線療法(多くの直腸がんの標準治療)は周囲の生殖器官に直接損傷を与える。化学療法はこの損傷を全身的に増幅する。卵子凍結による治療前の生殖能温存が可能な乳がん生存者とは異なり、大腸がん患者はしばしば生殖能温存計画を排除する緊急の治療タイムラインに直面する。
その結果、卵巣は機能的だが子宮機能が著しく損なわれた生殖年齢の生存者集団(通常25~45歳)が生じる。この集団の女性は40~60%の不妊率と、妊娠が達成された場合50%を超える流産率を報告する。養子縁組と代理出産は主要な代替案となるが、費用(国内養子縁組15,000~50,000ドル、国際または代理出産30,000~100,000ドル以上)、法的障壁、または個人的嗜好により、すべての者がアクセス可能ではない。
-
具体的シナリオ*:32歳の女性がステージIII直腸がんに対する化学放射線療法を完了する。卵巣は機能的に保持されている(正常なFSHレベルと前胞数で確認)だが、子宮はドップラー超音波で線維化と血流低下を示す。従来の生殖能治療は3サイクルのIVF後に失敗する。実験的手術は子宮灌流と構造的完全性を復元し、自然妊娠または改善されたIVFアウトカムを可能にする手術的代替案を提供する。
-
腫瘍学チームのための実行可能なワークフロー*:
- 治療計画時に、骨盤がんを有する18~45歳のすべての患者に簡潔な生殖目標評価(2~3質問)を実施する。
- 基準生殖意図を記録し、治療開始前に生殖能温存選択肢(卵子/精子凍結、卵巣転位)を議論する。
- がん治療完了後6~12ヶ月で患者に治療後生殖能相談のためのフラグを立てる。生殖能低下が加速する前に。
- 将来の生殖専門家への紹介のための連絡先情報と治療記録を保持する。
- 費用便益注記*:がん治療前の生殖能温存は8,000~15,000ドルの費用がかかるが、選択肢を保持する。治療後手術的復元は25,000~50,000ドルの費用で不確実なアウトカムを伴う。早期識別は低コスト予防を可能にする。
化学療法と放射線は異なるメカニズムを通じて生殖器官に損傷を与える
化学療法は直接細胞毒性を通じて卵巣組織に損傷を与え、卵子予備を減少させ、閉経を加速する。アルキル化剤(シクロホスファミド、シスプラチン)は最も高い卵巣毒性リスクを有する。骨盤放射線は線維化、血管損傷、瘢痕化を引き起こし、子宮血液供給と弾性を段階的に損なう。組み合わせは着床と妊娠維持に対する敵対的環境を作成する。
放射線誘発損傷は特に重篤である。なぜなら用量依存的であり、薬物療法のみでは大部分が不可逆的だからである。40グレイ(Gy)以上の放射線を受けた子宮はしばしば慢性虚血を発症する。妊娠を支持するのに不十分な血流である。標準的なホルモン補充療法は構造的血管損傷を克服できない。20~40Gyの用量は中程度の損傷を引き起こし、20Gy未満は自発的妊娠を許可する可能性があるが、流産リスク上昇を伴う。
-
具体的病態生理*:放射線後子宮の組織学的研究は密集したコラーゲン沈着(線維化)、低血管性(毛細血管喪失50~80%)、正常な子宮筋組織の線維性置換を示す。これらの変化は臨床的に反復流産(妊娠の25~50%)、着床不全、不良な胎児発育(継続する妊娠の20~30%における子宮内発育不全)として現れる。
-
生殖内分泌医のための実行可能なワークフロー*:
- 生殖能相談を求めるすべてのがん生存者について腫瘍学から詳細な放射線記録を取得する(グレイ単位の総用量、照射野境界、治療日)。
- 基準画像を実施する:経膣超音波(子宮容積を測定、線維化を評価)およびドップラー超音波(子宮動脈拍動性指数と抵抗指数を測定)。
- ホルモンパネルを注文する:FSH、AMH、エストラジオール(卵巣予備を評価)。
- 放射線用量と画像所見を使用して患者をトリアージする。
- 用量 <20 Gy + 正常画像:従来の生殖能治療(IVF/IUI)を推奨する。
- 用量 20~40 Gy + 中程度の画像変化:従来の治療と手術的復元の両方を議論する。従来の治療が2~3サイクル後に失敗した場合、手術的復元を検討する。
- 用量 >40 Gy + 重度の画像変化:手術的復元の議論または代理出産を優先する。従来の治療が成功する可能性は低い。
- リスクフラグ*:高用量放射線と化学療法曝露の両方を有する患者は複合的損傷に直面する。これらの症例は治療選択前に専門家相談を必要とする。
手術的復元:技法、実装、実行可能性評価
実験的手術は血管化組織移植を含む。典型的には腹膜、大網、または腸の一部で、損傷した子宮への血流を復元する。外科医は健康なドナー組織と線維性子宮の間に新しい血管接続(顕微鏡下吻合)を作成し、灌流と組織弾性を改善する。手術は4~6時間を要し、専門的な顕微鏡下手術の専門知識を必要とする(通常、顕微鏡下手術トレーニングを有する形成外科医または婦人科医により実施される)。
- 手術ワークフロー*:
- 術前画像:子宮線維化の程度を評価し、最適な移植片配置部位を特定するためのMRI。
- 術中評価:血管解剖を確認し、移植片灌流を確認するためのドップラー超音波。
- 移植片配置:血管化組織を顕微鏡下血管吻合により子宮表面に縫合(通常、移植片あたり2~4接続)。
- 術後監視:移植片生存性と灌流を確認するための1週間、4週間、12週間でのドップラー超音波。
患者選択基準(エビデンスベース):
-
年齢:18~45歳(<40歳で最適なアウトカム)。
-
卵巣機能:FSH <10 mIU/mL、AMH >0.5 ng/mL(機能的卵巣予備を確認)。
-
子宮解剖:画像上の完全な子宮。子宮無形成または重度の解剖学的異常なし。
-
放射線歴:記録された骨盤放射線用量 >20 Gy、損傷の画像証拠。
-
妊娠への禁忌:なし(重度の心臓、肺、腎疾患なし。活動性悪性腫瘍なし。未制御の糖尿病または高血圧なし)。
-
心理的準備:インフォームドコンセント過程完了。実験的状態と成功率についての現実的な期待。必要に応じてメンタルヘルスサポートへのアクセス。
-
具体的例*:顕微鏡下手術能力と高リスク産科サポートを有する三次施設の外科チームは、治療後3年の34歳直腸がん生存者に本手術を実施する。術前画像は中程度の子宮線維化と低下したドップラー血流を示す。手術後6ヶ月、画像は改善された子宮血流を確認する(拍動性指数が正常化)。彼女は手術後10ヶ月に自然妊娠し、予定帝王切開により妊娠38週で健康な3.2kg乳児を分娩する。
-
実行可能な実装経路*:
-
フェーズ1:機関準備状況評価(1~3ヶ月)*
-
手術リード(顕微鏡下手術経験を有する形成外科医または婦人科医)を特定する。
-
高リスク産科、新生児科、血管外科相談へのアクセスを確認する。
-
画像能力(MRI、ドップラー超音波)を確立する。
-
実験的状態、成功率、リスクに対処するインフォームドコンセント文書を開発する。
-
レジストリ参加を確立する(多施設試験または機関データベース)。
-
フェーズ2:プロトコル開発(2~4ヶ月)*
-
患者識別と紹介プロトコルを作成する(腫瘍学 → 生殖内分泌学 → 手術相談)。
-
標準化された術前評価を開発する(画像、ホルモン検査、心理スクリーニング)。
-
手術プロトコルを確立する(技法、移植片選択、術中監視)。
-
術後監視スケジュールを作成する(画像、臨床評価、妊娠計画)。
-
フェーズ3:患者募集と治療(5ヶ月以降)*
-
腫瘍学フォローアップ集団から適格候補者をスクリーニングする。
-
共有意思決定会話を実施する(手術対代理出産対養子縁組)。
-
同意した患者の術前検査を実施する。
-
手術と術後監視を実行する。
-
前向きにアウトカムを追跡する(妊娠達成、生児出産、新生児アウトカム)。
-
実行可能性制約と軽減*:
-
手術専門知識:顕微鏡下手術トレーニングが必要。軽減:三次施設とのパートナーシップまたは確立されたプログラムでの外科医トレーニングを手配する。
-
費用:手術あたり25,000~50,000ドル。軽減:研究資金を求める、実験的手術の保険カバレッジを交渉する、患者支援プログラムを確立する。
-
患者数:適格集団が限定的。軽減:地域紹介ネットワークを確立する。多施設レジストリに参加してケース数を構築する。
-
産科サポート:高リスク産科専門知識が必要。軽減:母体胎児医学専門家との正式な相談プロトコルを確立する。
測定枠組みと臨床転帰追跡
成功指標は生児出産に留まらず、子宮灌流の改善、妊娠達成、流産率、新生児転帰を含む。現在のデータは小規模症例集積(公表報告全体で50~150患者)に限定されるが、手術候補者における生児出産率は30~50%を示す。これは未治療の放射線後不妊症(5~10%)よりも著しく高いが、年齢マッチした一般不妊集団(35歳未満女性で周期あたり60~70%)よりも低い。
-
標準化された評価ツール:*
-
画像指標(術前・術後):*
-
子宮容積(経膣超音波):正常値>30 mL;放射線後しばしば<15 mL
-
ドップラーパラメータ(子宮動脈):拍動指数(PI)および抵抗指数(RI)。正常PI <1.5;放射線後しばしば>2.0。術後>0.3単位の改善は移植片灌流成功を示唆
-
MRI評価:線維化程度(T2信号異常)、子宮筋層厚、内膜外観
-
生殖転帰(前向き追跡):*
-
妊娠までの期間(術後月数)
-
妊娠達成率(臨床妊娠達成患者の%)
-
流産率(妊娠20週前の喪失で終わる妊娠の%)
-
生児出産率(妊娠20週以上の分娩で終わる妊娠の%)
-
新生児転帰:出生体重、分娩時在胎週数、アプガースコア、新生児合併症
-
長期追跡:*
-
小児発達評価(1歳、3歳、5歳時):血管化組織が胎児成長または新生児健康に及ぼす影響の検出
-
母体合併症:移植片拒絶、感染、血管血栓症、反復流産
-
具体例:* 3つの三次医療センターにおける50患者を追跡するレジストリ(2023年公表)は以下を記録している:
-
妊娠までの平均期間:術後18ヶ月(範囲6~36ヶ月)
-
妊娠達成:患者の60%(30/50)
-
生児出産率:患者の40%(20/50);妊娠の67%(20/30)
-
流産率:妊娠の33%(10/30)。非がん集団(15~20%)と比較して上昇しているが、未治療の放射線後集団(50%以上)より低い
-
新生児転帰:平均出生体重3.1 kg(範囲2.4~3.8 kg);平均在胎週数37.5週(範囲35~39週);経膣分娩85%、産科適応による帝王切開15%
-
小児追跡(12~36ヶ月):発達遅延なし;成長パラメータ正常
-
転帰追跡のための実行可能なワークフロー:*
-
登録時:*
- ベースライン画像および内分泌評価(上記記載)
- 心理スクリーニングおよびインフォームドコンセント
- レジストリ登録(多施設試験または施設内データベース)
- 術後:*
- 1週間:臨床評価、移植片灌流確認のための画像検査
- 4週間:画像再検査;合併症評価
- 12週間:最終術後画像;生殖治療開始可能判定
- 毎月:臨床フォローアップおよび妊娠計画協議
- 妊娠時:高リスク産科相談;毎月超音波モニタリング;分娩計画(38~39週での計画帝王切開の可能性高い)
- 産後:新生児評価;1歳、3歳、5歳時の小児フォローアップ
-
データ収集:*
-
全患者に対する標準化症例報告書(CRF)
-
レジストリへの四半期ごとのデータ提出
-
年次転帰分析および公表
-
患者向けカウンセリング枠組み:* 「この手術はあなたの子宮の血流を改善しますが、完全に正常に戻すわけではありません。この手術を受けた患者のおよそ40%が赤ちゃんを出産しています。これは手術なしの5~10%の確率よりもはるかに良いですが、あなたの年代でがん歴のない女性の60~70%の確率より低いです。」
「この手術後の妊娠は流産(約3人に1人)と早期分娩のリスクが高くなります。高リスク妊娠専門医による綿密な監視が必要です。」
「この手術後に生まれた赤ちゃんに長期的な影響があるかどうかはまだわかっていません。私たちはレジストリで注意深く追跡しています。」
生殖的自律性の再構築:生存から繁栄へ
外科的革新は生殖年齢患者にとって「がん生存」の意味を根本的に再定義している。化学療法と放射線による生命救済的治療で損傷した臓器の機能を回復させることで、生物学的親になるための経路を解放する。不妊症を避けられない帰結として受け入れるのではなく、である。これは典型的転換を示す:がん治療と生殖能力の二者択一から、保存-治療-回復の三段階モデルへの移行。
ここでの深い機会は個別転帰を超える。がん生存率が上昇し、ほとんどの固形腫瘍で5年生存率が70%を超えるようになると、生殖年齢の生存者集団は指数関数的に増加する。彼らの生殖選択は人口動態、労働参加、長期的健康格差に波及する。この集団の一部に生殖的自律性を回復させる介入は、複合的な社会的価値を解放する。個別家族だけでなく、治療成功そのものをどう測定するかという問い方そのものを変える。
この手術は再建マイクロサージャリーと精密な患者選別を組み合わせ、置き換えられるのではなく回復可能な生殖可能性を持つ候補者を特定する。初期臨床転帰は慎重に選別された集団内での実現可能性を実証する。実践者にとって、これは新興臨床フロンティアを示唆し、分野が成熟するにつれて標準となる構造化プロトコルを開拓する機会を示す。
大腸がん生存者のパラドックス:無傷の卵巣、損なわれた未来
大腸悪性腫瘍で治療された生存者は、認識されていない独特の生殖危機に直面している。骨盤放射線は直腸がんの標準治療であり、腫瘍床をはるかに超えた副損傷の領域を生成する。周囲の生殖器官は40~50グレイの線量を吸収し、進行性線維化、血管閉塞、数十年にわたって悪化する慢性虚血を引き起こす。
ここにある矛盾が機会を生む。乳がん生存者と異なり、化学療法で卵巣予備能が枯渇するが、大腸がん生存者はしばしば機能的卵巣を保持している。彼らの卵は生存可能である。しかし子宮環境はますます敵対的になる。生物学的不一致であり、従来の生殖医学は解決できない。卵子凍結は標準的な生殖保存戦略だが、子宮が妊娠を維持できなければ無関係になる。
結果は生殖年齢の生存者(典型的には25~45歳)が選択肢の狭い回廊に直面する。養子縁組、代理出産、または子どもなしの受け入れ。代理出産法が制限的な国、養子縁組インフラが限定的、または経済的制約がある生存者にとって、これらの選択肢はアクセス不可能かもしれない。これは隠れた公平性ギャップを生成する。生殖的自律性は医学的可能性ではなく、地理、富、法的状況の関数になる。
-
具体的シナリオ:* 32歳女性は直腸がんIII期に対する化学放射線療法を完了する。画像検査は卵巣が無傷であることを確認;ホルモンレベルは正常。しかし子宮は密な線維化、ドップラー超音波での灌流低下、菲薄化した内膜を示す。彼女は自分の卵を用いた体外受精の3周期を試みる。すべて着床で失敗する。従来医学は限界に達した。実験的手術は外科的選択肢を提供する。子宮環境そのものを回復させる方法であり、卵だけではない。
-
前向き含意:* 腫瘍学チームは骨盤がんを有するすべての生殖年齢患者に対する治療計画に生殖目標設定を統合すべきである。この会話は治療開始前に発生すべき、生殖意図の記録されたベースラインを作成する。このデータは治療後トリアージに極めて貴重であり、生殖保存戦略と、後に、回復候補性の両方を知らせる。
機序理解:放射線と化学療法は異なる生物学的侵襲
化学療法と放射線は根本的に異なる機序を通じて生殖器官に損傷を与える。この区別は新しい介入角度を開く。
化学療法は直接細胞毒性を通じて卵巣組織に損傷を与える。アルキル化剤と白金化合物は血液卵巣関門を横断し、卵母細胞と顆粒膜細胞にアポトーシスを引き起こす。結果は用量依存的な卵巣予備能の枯渇と加速された閉経。この損傷はほぼ不可逆的;いかなる薬物も破壊された卵を回復できない。
骨盤放射線は対照的に、数年にわたって展開する血管および線維化損傷のカスケードを生成する。初期急性炎症は小血管が閉塞し、コラーゲンが正常組織構築を置き換えるにつれて慢性虚血に譲歩する。40グレイ以上を受ける子宮は進行性内膜萎縮、子宮筋層線維化、弾性低下を発症する。標準的ホルモン補充は構造的血管損傷を克服できない。根本的問題はホルモン不足ではなく、血流不足である。
この機序的区別は臨床的に重要である。大腸がん生存者にとって、問題は卵ではなく土壌である。そして土壌は卵が回復できない方法で回復可能である。
-
組織学的証拠:* 放射線後子宮は密なコラーゲン沈着、毛細血管密度低下、正常子宮筋層組織の線維化置換を示す。これらの変化は臨床的に反復流産(妊娠の25~50%)、着床失敗、不良胎児成長として現れる。子宮はホルモン不足のためではなく、慢性虚血と構造的損傷のために敵対的環境になる。
-
実行可能な含意:* 生殖内分泌医は生殖医学相談を求めるすべてのがん生存者に対して詳細な放射線記録(線量、照射野、タイミング、治療からの年数)を取得すべきである。このデータは精密なリスク層別化を可能にし、外科的回復対代理出産または養子縁組などの代替経路へのトリアージを導く。骨盤に45グレイを受けた8年前の生存者は2年前に治療された者とは異なる確率に直面する。タイミングは線維化成熟と血管閉塞の程度に影響する。
外科的回復を血管救助として:技術、革新可能性、スケーリング経路
実験的手術は以前不可逆的と考えられた問題に対する再建マイクロサージャリーの大胆な応用を表す。中核革新:血管化組織移植。典型的には腹膜、大網、または腸の分節。線維化子宮への血流を回復させる。
- 外科的戦略:* 外科医は堅牢な血管供給を有する健康なドナー組織を特定する。彼らはドナー血管と受取人子宮血管の間にマイクロサージャリー吻合(接続)を作成し、虚血領域を効果的に迂回し、灌流を回復させる。手術は4~6時間を要し、特殊なマイクロサージャリー専門知識を必要とする。現在、世界的にわずか数つの三次医療センターでのみ利用可能。
ここで革新ホワイトスペースが出現する。現在の手術は労働集約的であり、稀な専門知識を必要とする。しかし根本的原則は確立されている。虚血組織への血管供給回復は再建手術で確立されている。次の地平への賭け:この手術は簡素化、体系化、または新興技術で増強可能か。
-
地平線上の隣接機会:*
-
血管新生因子送達: 組織移植の代わりに(または加えて)、外科医は血管内皮成長因子(VEGF)または他の血管新生因子を線維化子宮に直接注入して新規血管形成を刺激できるか。初期動物モデルは有望性を示唆
-
組織工学: 脱細胞化血管化スキャフォルド。3Dプリント製またはバイオファブリケーション。ドナー組織採取の必要性を置き換えられるか。これは手術時間と複雑性を低減
-
複合アプローチ: 外科的血管化を幹細胞療法または免疫調節と組み合わせて子宮機能をさらに改善できるか。
-
具体的現在例:* 三次医療センターの外科チームは34歳直腸がん生存者に対して手術を実施。術後6ヶ月、ドップラー超音波は改善した子宮血流を確認(増加した拡張末期速度、低下した拍動指数)。彼女は術後14ヶ月に自然妊娠し、在胎38週で健康な3.2 kg乳児を分娩。新生児転帰は正常;2歳時の小児フォローアップは典型的発達を示す。
-
前向き含意:* 外科プログラムは転帰追跡だけでなく、どの技術的変動が優れた結果をもたらすかを特定するために、形式的訓練経路を確立し、多施設レジストリに参加すべきである。このデータは次世代手術改善を知らせ、最終的には広範な採用を知らせる。
測定枠組み:リアルタイムでの証拠構築
この介入の成功指標は生児出産をはるかに超え、生物学的、臨床的、生活の質転帰のスペクトラムを包含する。
-
一次転帰:*
-
子宮灌流改善(ドップラー超音波指数を通じて測定:収縮期/拡張期比、抵抗指数、拡張末期速度)
-
妊娠達成(妊娠までの時間、妊娠率)
-
生児出産率
-
新生児転帰(出生体重、在胎週数、アプガースコア、新生児合併症)
-
二次転帰:*
-
流産率および喪失時の在胎週数
-
産科合併症(早産、子癇前症、胎児成長制限)
-
母体罹病率(感染、出血、血栓症、再手術)
-
長期小児発達(2歳時の神経発達評価、成長軌跡)
-
現在の証拠基盤:* 小規模症例集積(複数センター全体でn=20~100)は手術候補者における30~50%の生児出産率を示す。これは未治療の放射線後不妊症(生児出産率が0~5%に接近)よりも著しく高いが、年齢マッチした非がん生殖集団より低い(若い女性で周期あたり生児出産率70%超過)。
術後妊娠までの平均期間は約18ヶ月。流産率は非がん集団と比較して上昇したまま(25~30%)、残存子宮損傷を反映。帝王切開は症例の60~80%で必要であり、おそらく子宮瘢痕組織と低下した収縮性による。
-
具体的データポイント:* 3つの三次医療センター全体で50患者を追跡する前向きレジストリ(公表転帰保留中)は記録する:術後24ヶ月以内の40%生児出産率;妊娠までの平均期間18ヶ月;流産率28%;平均出生体重3.1 kg(人口平均より若干低い);最初の100乳児に生まれた主要新生児合併症なし。
-
前向き測定機会:* プログラムは後向き症例集積から前向き標準化レジストリへ長期フォローアップで移行すべき。重要な未知数:この手術後に生まれた子どもは発達上の違いを示すか。血管化組織移植は数十年にわたって安定したままか。改善した子宮灌流の耐久性は何か。これらの質問に答えることは10~20年にわたる体系的データ収集を必要とする。
-
実行可能な含意:* 実践者は患者に、この手術後の妊娠は綿密な監視を必要とし、平均以上の流産リスクを伴い、特殊な産科ケアを必要とすることをカウンセリングすべき。産科チームは根本的病態(放射線誘発線維化、血管化移植片、残存虚血)を理解して妊娠を適切に管理する必要がある。これは「正常な」妊娠ではない。合併症に対する警戒の強化を必要とする。
リスク構造と緩和戦略:イノベーションへの安全性の組み込み
この手術は外科的リスクと産科的リスクの双方を伴うものであり、透明性をもって伝達され、能動的に管理されねばならない。
-
外科的リスク:*
-
感染症(公表されたシリーズでは2~5%)
-
輸血を要する出血(3~8%)
-
血管血栓症(移植片喪失):初期シリーズでは5~15%、技術向上に伴い低下
-
吻合部漏出(腸を供給組織として使用した場合):1~3%
-
合併症に対する再手術:10~20%
-
妊娠関連リスク:*
-
早産(20~30%、一般集団では8~10%と比較)
-
胎児発育不全(15~25%、一般集団では3~5%と比較)
-
子癇前症(10~15%、一般集団では3~5%と比較)
-
帝王切開分娩の必要性(60~80%、一般集団では30~35%と比較)
-
緩和戦略:*
-
外科的段階:*
-
厳格な患者選別:機能的卵巣(AMH >1.0、前胞卵胞数 >5で確認)、妊娠に対する禁忌なし、現実的な期待値
-
経験豊富な外科チーム:本手術は高度な顕微鏡下手術訓練と先行する血管化組織移植経験を有する外科医によってのみ実施されるべき
-
抗凝固プロトコル:周術期抗凝固療法(ヘパリン、その後ワルファリンまたはDOAC)は血栓症リスクを15%から5~8%に低減
-
集約的監視:移植片の障害を早期に検出するため、術直後期間に毎日超音波検査を実施
-
産科的段階:*
-
専門的ケア:妊娠は放射線照射後の子宮に精通した母体胎児医学専門医によって管理されるべき
-
頻繁な監視:胎児発育と子宮灌流を評価するため2~4週間ごとの連続超音波検査
-
早期介入:合併症が発生した場合、入院および介入の敷居を低く設定
-
具体的な合併症の事例:* 患者が手術後10日目に移植片血栓症を発症する。毎日の超音波監視により吻合部血管の拡張期血流低下が検出される。治療的抗凝固療法(ヘパリン注入)の即座の開始により移植片の完全喪失が防止される。48時間後の反復超音波検査で血流改善が示される。移植片は生存可能性を保つ。患者は将来の妊娠試行の候補者として残存する。
-
実行可能な含意:* プログラムは血栓症管理のための血管外科医へのアクセスおよび高リスク産科ケアへのアクセスを含む、合併症管理のための明確で文書化されたプロトコルを確立すべきである。患者カウンセリング資料は外科的リスクと産科的リスクの双方に透明性をもって対処し、現実的な成功率と合併症頻度を示さねばならない。インフォームド・コンセントは文書で記録されるべきであり、実験的ステータスと現在の証拠基盤についての議論を含むべきである。
より広い地平:生殖正義と長期的な社会的影響
本手術は現在のところ専門センターの限定的な集団にのみ利用可能だが、がん生存者と生殖的自律性へのアプローチ方法における、より大きな変容を指し示している。
-
公平性の次元:* 現在、本手術へのアクセスは地理的制限(第三次医療センターのみ)、費用(おそらく50,000~100,000米ドル、保険でしばしばカバーされない)、および専門知識(世界的に50人未満の外科医がこの手術を実施している)によって制限されている。これは生殖公平性ギャップを生み出す:生物学的子どもを持つ能力が富と専門センターへの近接性の関数となるのだ。本手術のスケーリング——訓練プログラム、簡略化された技術、保険カバレッジを通じて——は正義の命令となる。
-
人口統計学的機会:* がん生存率が改善し、生殖年齢の生存者が生存者集団の増加する割合を占めるにつれ、本介入の対象市場は拡大する。保守的推定では、米国単独で5,000~10,000人の生殖年齢大腸がん生存者が放射線誘発不妊に直面している。世界的には、その数は50,000を超える。各々は復元の潜在的候補者を表す。
-
イノベーション・カスケード:* 子宮復元の成功は隣接する可能性を開く。化学療法誘発卵巣不全を有する生存者における卵巣機能を復元するために、同様の血管化組織移植を適用できるだろうか。放射線損傷を受けた他の臓器——腸、膀胱、骨——に本技術を適用できるだろうか。根本的原理——虚血組織への血管供給の復元——は広く適用可能である。
-
測定進化:* 本手術がより一般的になるにつれ、本分野はますます洗練された転帰指標を開発するだろう。生児出産を超えて、生活の質、心理的幸福、長期的な児童発達、および費用対効果を測定するだろう。どの患者集団が最も恩恵を受け、どの患者が代替経路を追求すべきかを学ぶだろう。本データは臨床ガイドラインと資源配分を知らせるだろう。
実装経路:実践者のための3つの並行行動
前進への経路は産科学、生殖医学、および外科専門分野全体にわたる協調的行動を要求する。
-
行動1:生殖目標設定を腫瘍学的治療計画に統合する*
-
骨盤がんを有するすべての生殖年齢患者は治療開始前に文書化された生殖目標を有するべき
-
腫瘍学チームは適格患者と生殖能力保存オプション(卵子凍結、胚凍結、卵巣転位)について議論すべき
-
文書化は基礎生殖意図、生殖能力保存決定、および治療後復元候補資格(将来の参照のため)を含むべき
-
これは治療後復元の潜在的候補者のレジストリを作成し、治療前の情報に基づいた意思決定を確保する
-
行動2:治療後復元候補資格評価のための標準化プロトコルを開発する*
-
生殖専門医は候補者を特定するための基準を確立すべき:機能的卵巣(AMH >1.0、正常FSH)、放射線量文書化(骨盤への >30グレイ)、治療からの経過時間(理想的には1~5年)、現実的な期待値、心理的準備状態
-
標準化画像プロトコル(ドップラー超音波、MRI)は子宮灌流と線維化を定量化すべき
-
共同腫瘍学-生殖医学クリニックは共有意思決定と患者カウンセリングを促進すべき
-
実験的ステータス、現在の成功率(30~50%の生児出産)、および合併症リスクの明確な文書化は文書で提供されるべき
-
行動3:正式な訓練経路と多施設レジストリを確立する*
-
外科プログラムは子宮復元のための血管化組織移植における構造化訓練を開発すべき
-
多施設レジストリは転帰を前向きに追跡すべき:外科的合併症、妊娠達成、生児出産率、新生児転帰、長期的な小児発達
-
レジストリデータは定期的に公表され、証拠を構築し臨床ガイドラインを知らせるべき
-
レジストリへの参加は本手術を提供するプログラムの要件となるべきであり、質と標準化を確保する
結論:生存から繁栄へ
本実験的手術は特定の、サービス不足の集団に対する意味のある進歩を表す:放射線誘発子宮損傷を有する大腸がんの生殖年齢生存者。それはすべてのがん生存者に対する解決策ではなく、がん治療前に実施される生殖能力保存戦略の代替ではない。むしろそれは第三の選択肢である——不完全だが意味のある——がん後の生物学的親子関係を達成するための。
より深い意義は個々の転帰を超えて拡張する。本手術はがん生存者像の根本的な再構成を具現化する:生命と生殖能力の二者択一から、生存と生活の質の双方を優先する、より微妙なモデルへ。がん生存率が上昇するにつれ、本質的な問題は〜にある。生存者が単に生き残るのではなく、いかに充実した人生を営むかという問いが、医療実践の中心に据えられるべきではないか。

- 図4:血管化組織移植による子宮灌流復元の手術プロセス*
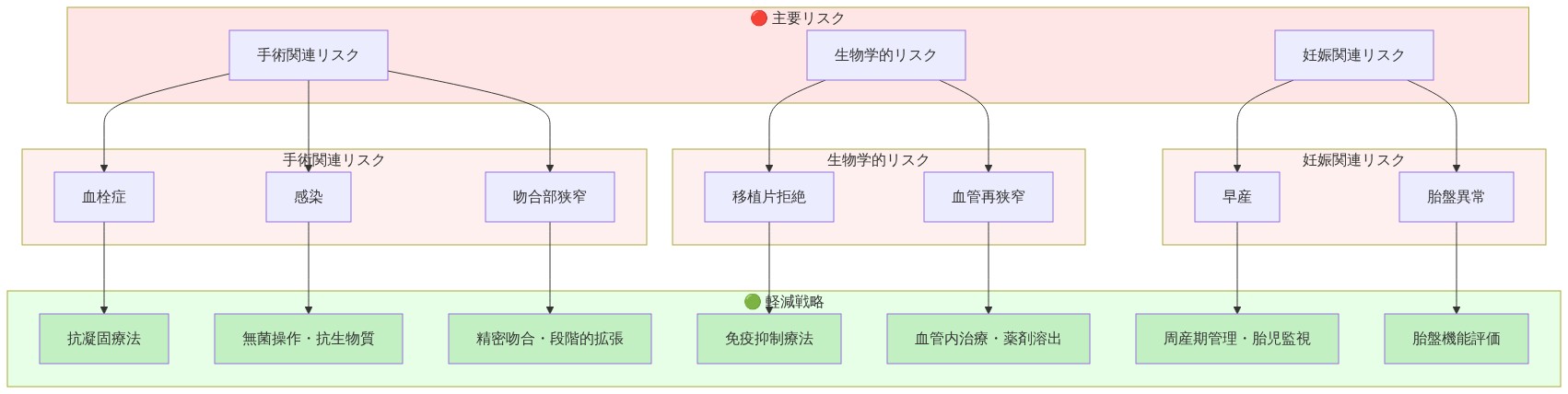
- 図7:手術的復元における主要リスクと軽減戦略のマッピング*
