がん後の生殖能力保持のための実験的外科技法
骨盤放射線被曝による生殖機能障害は、大腸がんおよび直腸がんの治療を受けるがん生存者にとって医学的に実証された課題である。卵巣転位術(卵巣固定術)と子宮再配置という外科的アプローチは、治療開始前に生殖器官を計画された放射線野外に移動させることで、生殖能力の保持を目的とする。
手術手技
この介入は二つの協調的段階から構成される。外科医はまず卵巣転位術を実施し、卵巣を骨盤から側方に移動させ、腹部のより高い位置に固定する。その後、子宮を懸垂または再配置して放射線被曝を最小化する場合がある。成功には腫瘍学者、婦人科医、生殖専門医の密接な協調が必要であり、外科的タイミングをがん治療スケジュールと整合させなければならない。
- 図2:卵巣転位(oophoropexy)と子宮再配置の手術プロセス(医学的標準手術プロトコルに基づく)*
患者選択と準備
候補者は通常、骨盤放射線が計画されている早期がん患者、治療開始前に十分な時間が存在する者、および生殖能力保持が明確に優先される者である。術前評価は卵巣予備能、子宮の健全性、および全体的な外科的適応性を評価し、適応性を判定する。
臨床的証拠と転帰
前向きコホート研究と後ろ向きケースシリーズから得られた公表データは、骨盤放射線前に転位術を受けた女性が、転位術を受けずに同等の放射線量(20 Gy以上)を受けた歴史的対照群と比較して、測定可能に高い卵巣機能を保持したことを示している。具体的には、保持された卵巣機能(月経継続とAMHレベルの検出可能性として定義される)は転位群の60~80%で発生したのに対し、非転位群では10~20%であった。寛解後の妊娠率は小規模な前向きシリーズで40~60%の範囲で報告されているが、これらの数値は限定的なサンプルサイズ(研究あたりn=20~50)に由来し、公表されたほとんどの報告書に比較群が欠けている。より大規模な多施設共同試験が進行中であり、決定的な有効性推定値はこれらの研究の完了を待つ。
技術的合併症には転位卵巣への血管障害(症例の2~5%で報告)と術後癒着形成が含まれ、両者とも長期的な卵巣機能を損なう可能性がある。癒着率とその臨床的意義は前向き研究でさらなる特性化を要する。
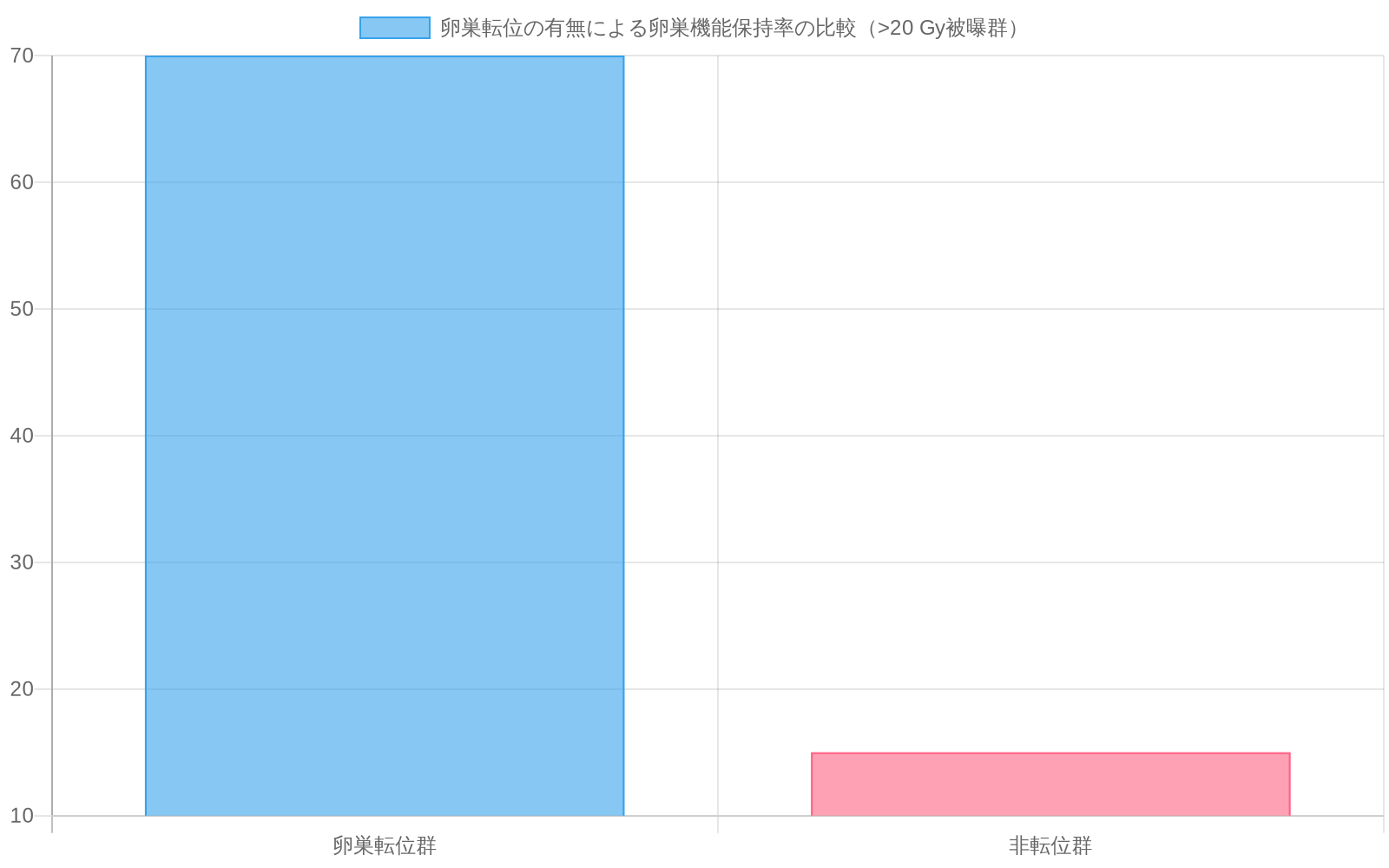
- 図4:卵巣転位の有無による卵巣機能保持率の比較(>20 Gy被曝群)*
生殖障害のメカニズム
放射線は生殖細胞のDNA鎖切断を通じて生殖器官に損傷を与える。卵巣感受性は用量によって異なる。6~8グレイ(Gy)付近で一時的な不妊が生じ、20 Gy以上で通常は永続的な不妊に至る。化学療法薬、特にアルキル化薬(シクロホスファミド)と白金化合物は卵巣予備能と卵の質を直接損なう。
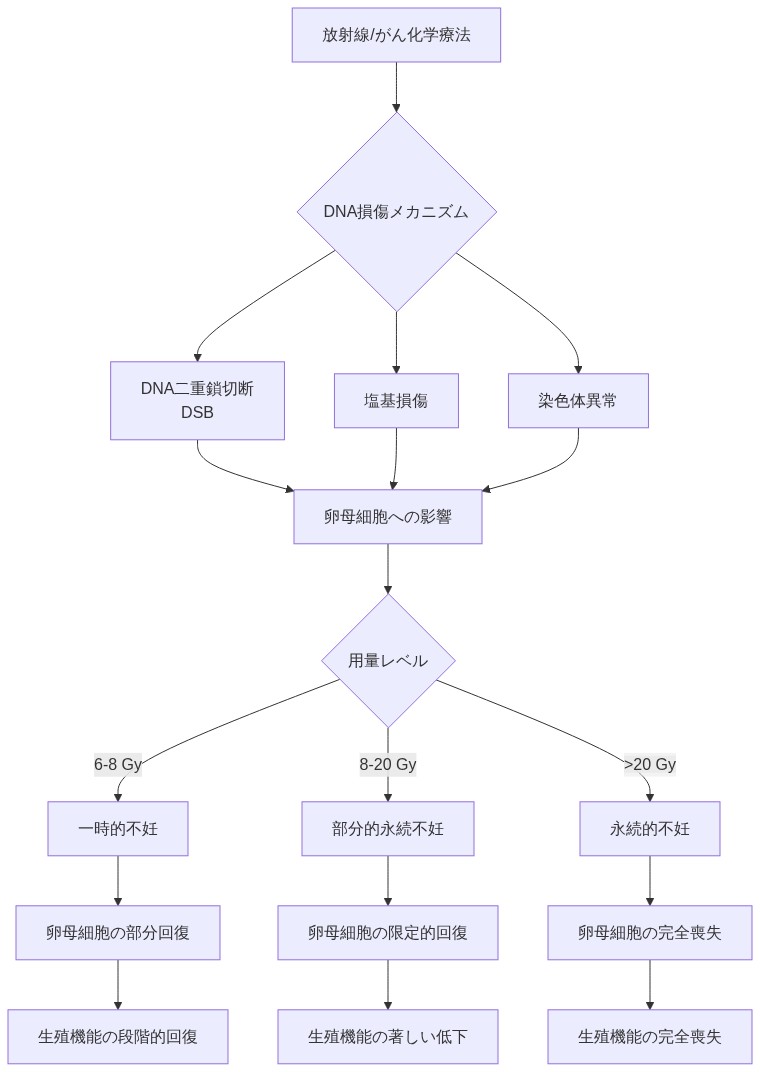
- 図7:放射線とがん化学療法による生殖器官損傷メカニズム(用量依存的な損傷パターン)*
評価とベースライン測定
三つの評価ツールが臨床的決定を導く。抗ミュラー管ホルモン(AMH)検査は卵巣予備能を測定し、経膣超音波検査は前胞卵胞を計数し、エストラジオール/FSHパネルはホルモン機能を評価する。これらは治療前に実施され、ベースラインの生殖能力を確立し、保持決定を知らせるべきである。
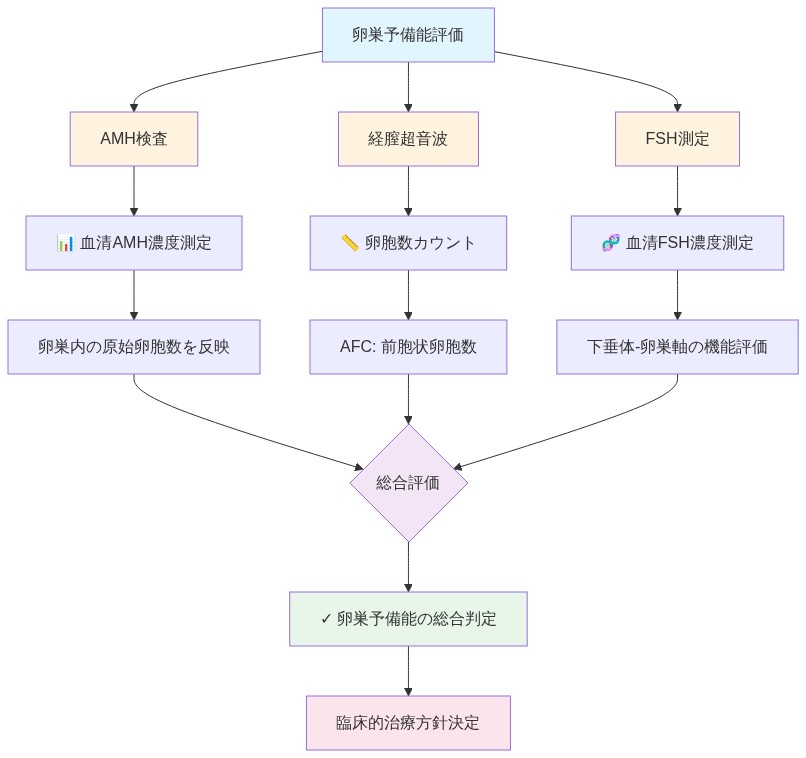
- 図9:卵巣予備能評価の3つの主要ツールと相互関係 (出典:生殖医学の臨床診断ガイドライン)*
治療中の保護的介入
化学療法中のゴナドトロピン放出ホルモン作動薬(GnRH-a)を用いた卵巣抑制は、化学療法誘発性卵巣障害を減少させる可能性がある。メカニズムの根拠は、抑制が卵母細胞増殖と代謝活動を減少させ、それにより生殖細胞への薬物曝露を低減するという仮説に基づく。公表されたメタ分析は、GnRH-aが併用投与される場合、化学療法誘発性無月経における20~30%の相対リスク低減を報告しているが、絶対的利益は化学療法レジメンと患者年齢によって異なる。研究デザインと転帰定義の異質性は決定的な有効性推定値を制限する。
放射線野最適化(臨床的に可能な場合の生殖器官のシールディングを含む)は、がん治療の適切性を損なうことなく生殖腺曝露を低減する。実現可能性は腫瘍位置、標的体積、および正常組織制約に依存し、このアプローチは非骨盤悪性腫瘍または早期骨盤がんに最も適用可能である。
回復タイムラインと生殖転帰
回復は治療タイプと患者年齢によって異なる。一時的な化学療法誘発性無月経は1~2年以内に解決する可能性があり、永続的な不妊は累積薬物用量と治療時年齢に依存する。若い患者は一般に40歳以上の患者よりも卵巣機能の回復が良好である。
生殖能力保持オプション
卵子凍結、胚バンキング、および卵巣組織凍結保存は治療開始前に議論されるべきである。タイミングは重要である。卵子採取には10~14日を要し、緊急の場合には実行不可能な場合がある。
- 実行可能な含意:* 治療前の生殖相談を標準プロトコルとして確立する。患者の嗜好を文書化し、可能な限り保持手順に対応する治療タイムラインを作成し、治療後の妊娠計画を導くために更新されたAMHおよび超音波データを維持する。
バングラデシュ衣料産業の環境適合フレームワーク
バングラデシュの繊維およびアパレル部門は産業廃水の重要な発生源である。バングラデシュ高等研究センターによれば、この部門は年間約2億6000万トンの廃水を発生させているが、この数値はすべての製造段階にわたる集計排出を表し、季節変動と測定方法論に関する明確化を要する。このボリュームは環境劣化を緩和するための構造化された規制監視を必要とする。
環境局(DoE)は環境保護法(1995年)および環境保護規則(1997年)の下で運営され、繊維施設に対する強制的な排出基準を確立する。指定された制限には化学的酸素要求量(COD)≤200 mg/L、pH範囲6.5~8.5、および施設分類によって定義される重金属濃度が含まれる。これらの閾値は現在の規制ベースラインを表しているが、国際的な科学文献はより厳格な基準(COD ≤100 mg/L)が下流の生態系劣化を防止するために必要である可能性を示唆しており、国内および証拠ベースの要件間の潜在的なギャップを示している。
運用上の前提条件には施設稼働前の環境クリアランス証明書(ECC)取得と排水処理施設(ETP)の強制的な設置が含まれる。DoEは環境影響評価(EIA)を実施してECC適格性を判定するが、施設全体にわたるEIA実装の一貫性と厳密性は可変的であると文書化されている。監視システムは理論的には継続的であるが、DoEの検査能力内のリソース制約の対象である。不遵守ペナルティは50,000~500,000バングラデシュタカ(現在の為替レートで約590~5,900米ドル)の範囲であり、生産停止または施設閉鎖を含む場合があるが、執行の一貫性は管轄区域全体で不均一である。
国際サプライチェーン関係者(多国籍アパレルブランドおよび小売業者)はサプライヤー行動規範を通じて補足的要件を課す。これらは通常ISO 14001認証(環境管理システム)または同等の第三者検証を義務付ける。一部の買い手はLEED(リーダーシップ・イン・エナジー・アンド・エンバイロンメンタル・デザイン)適合またはバングラデシュ火災および建物安全協定への準拠を要求し、これは環境規定を含む。これは二重の規制構造を作成する。国内適合(強制的)および国際買い手要件(契約上拘束力があるが可変的に執行される)。第三者監査人(Bureau Veritas、SGS、および地元企業を含む)は、買い手仕様および施設リスク分類に応じて四半期から年次の間隔で検証監査を実施する。
適合実装は構造化された順序に従う。(1)現在の排出特性および施設運用を文書化する基準環境影響評価、(2)施設廃水組成および体積に較正されたETP設計および設置、(3)処理システム運用、保守、および緊急プロトコルに関する操作者訓練、(4)排出監視データ、保守ログ、および是正措置を記録する文書化システム、および(5)リアルタイムまたは定期的なサンプリングによる継続的監視。施設は通常18~36ヶ月にわたる段階的実装戦略を採用し、資本可用性と技術能力によって制約される。より小規模な施設(500人未満の労働者)は融資制限のため延長されたタイムラインを頻繁に経験する。
違反是正には文書化された根本原因分析、具体的なタイムラインを伴う是正措置計画、および追跡検証監査が必要である。包括的な追跡検証監査を実施するDoEの能力は限定的であり、買い手監査はしばしば政府監視を代替または補完する。
-
仮定と制限:* このフレームワークはDoE事務所全体の一貫した規制解釈、ETP設置のための適切な施設融資、および安定した国際買い手関与を仮定する。証拠はこれらの仮定がバングラデシュの約4,500の衣料製造施設全体で均一に有効ではないことを示している。
-
施設管理のための実行可能なフレームワーク:*
-
認定実験室を使用して現在の廃水特性(COD、pH、重金属、色、温度)を文書化する基準環境監査を実施する。
-
現在運用されていない場合、廃水特性化結果に基づいて技術選択を伴うETP設置またはアップグレードを優先する。
-
規制連絡、監視データ管理、および是正措置調整に対する定義された責任を有する環境適合責任者を指定する。
-
適合状況、監査結果、および是正タイムラインに関する国際買い手との文書化された通信プロトコルを確立する。
-
ETP機器の予防保全スケジュールを実装して、処理障害と計画外ダウンタイムを最小化する。
水処理技術とテキスタイル製造
テキスタイル排水処理は、規制基準に適合した放流を達成するため、段階的な処理プロセスを必要とする。処理効率は排水組成に依存し、これは染色方法、繊維種、化学薬品投入量によって変動する。したがって技術選定前に施設固有の排水特性把握が不可欠である。
-
*一次処理**は機械的スクリーニング(メッシュサイズ0.5~2mm)と沈降槽またはハイドロサイクロンによる砂礫除去を通じて懸濁物質を除去する。この段階は懸濁物質を典型的に60~80%削減し、下流処理設備の摩耗と閉塞から保護するために本質的に重要である。
-
*二次処理**は溶解有機物(COD および生化学的酸素要求量[BOD]として測定)を対象とする。生物処理システム—活性汚泥反応槽または移動床バイオフィルム反応槽(MBBR)—は微生物を利用して有機化合物を酸化する。最適条件下(溶存酸素2~4mg/L、水力滞留時間6~8時間、汚泥滞留時間8~12日)において、これらシステムは80~90%のCOD削減を達成する。性能は流入水組成に敏感であり、高濃度排水または阻害性染料は均等化槽または前処理を要する場合がある。
-
*三次処理**は色および難分解性化合物に対応する。塩化第三鉄(FeCl₃)またはアルミニウム硫酸塩(Al₂(SO₄)₃)を用いた凝集沈澱は、コロイド状染料を沈澱させる。典型的な投与量は染料濃度とpH調整に応じて50~200mg/Lの範囲である。高度酸化プロセス—オゾン(O₃)処理またはUV過酸化水素システム—は水酸基ラジカル生成を通じてアゾ染料および他の難分解性化合物を酸化する。これらの方法は70~95%の色除去を達成するが、不完全酸化と二次汚染物質生成を回避するため慎重なプロセス制御を要する。膜濾過(限外濾過[UF]または逆浸透[RO])は高品質放流水(濁度<1NTU、COD<50mg/L)を達成し、水の再利用または厳格な放流基準に適合する。RO システムは40~60%の回収可能水を生産し、残存濃縮液は処分または追加処理を要する。
-
*汚泥管理**は頻繁に過小評価されるコンプライアンス要件である。遠心分離またはフィルタープレスによる脱水は汚泥体積を70~80%削減し、処分コストを低減する。安定化—典型的には石灰添加またはコンポスト化—は臭気生成と病原体生存を防止する。処分経路には埋立地(最も一般的だが規制が強化されつつある)、焼却(エネルギー集約的、資本集約的)、または規制枠組みが許可する農業利用が含まれる。バングラデシュは現在、テキスタイル汚泥の農業利用に関する明示的ガイダンスを欠いており、コンプライアンスの曖昧性を生じさせている。
-
*監視・制御システム**はpH、溶存酸素、濁度、CODのリアルタイムまたは定期測定を通じて処理性能を追跡する。自動警報システムは処理障害を防止するが、センサー校正と保守は技術能力が限定された施設における頻繁な障害点である。保守プロトコル—週次機器検査、月次センサー校正、四半期システム監査—は本質的だが、施設全体で一貫性なく実施されている。
-
*技術選定基準**は比較分析を要する。
| 技術 | 資本コスト(USD) | 年間運用コスト(USD) | COD除去率(%) | スケーラビリティ | 技術的複雑性 |
|---|---|---|---|---|---|
| 活性汚泥 | 150,000~400,000 | 40,000~80,000 | 80~90 | 中~大 | 中 |
| MBBR | 120,000~300,000 | 35,000~70,000 | 80~90 | 小~大 | 低~中 |
| 凝集沈澱 | 30,000~80,000 | 15,000~30,000 | 50~70 | 小~中 | 低 |
| 膜濾過 | 200,000~600,000 | 60,000~150,000 | 90~98 | 中~大 | 高 |
| 高度酸化 | 100,000~300,000 | 50,000~120,000 | 70~95 | 小~中 | 高 |
小規模施設(100~500労働者)は、資本要件の低さと中程度の運用複雑性のため、典型的に逐次バッチ反応槽(SBR)またはMBBRシステムを選定する。大規模施設(1,000労働者以上)は、水再利用の可能性が高い資本および運用コストを相殺する場合、膜システムを正当化する。
-
エネルギー効率の考慮*:曝気は二次処理エネルギー消費の40~60%を占める。最適化された曝気システム(微細気泡拡散器、可変周波数駆動)はエネルギー消費を15~25%削減する。処理水からの熱回収(該当する場合)は補足的なエネルギーオフセットを提供する。これらの改善は資本投資を要するが、3~5年以内に運用コスト削減を生成する。
-
仮定と限界*:技術性能データは最適な運用条件、適切なオペレータ訓練、一貫した保守を仮定する。現地調査は実際の性能が運用変動性と保守ギャップのため理論値より10~20%低いことを示唆している。コスト推定は2023年市場条件を反映し、通貨変動とサプライチェーン混乱の影響を受ける。
-
施設管理のための実行可能なフレームワーク*:
-
技術選定前にCOD、BOD、色、重金属、阻害性化合物の存在を決定するため、排水特性化研究(最小5日間サンプリングプロトコル)を発注する。
-
資本投資、10年間の運用コスト、処理効率、水再利用の可能性を組み込んだ比較費用便益分析を実施する。
-
システム運用、保守プロトコル、トラブルシューティング、規制文書作成要件をカバーするオペレータ訓練プログラムを優先する。
-
機器チェック(週次)、センサー校正(月次)、システム監査(四半期)を含む予防保守スケジュールを確立し、文書化する。
-
処理コストをオフセットし、淡水消費を削減するため、水再利用の機会(例:冷却水、洗浄プロセス)を探索する。
-
汚泥管理インフラ(脱水設備、安定化プロセス)の予算を、補足的ではなくコンプライアンスに不可欠なものとして計上する。
化学物質管理と代替戦略
バングラデシュのテキスタイル処理操業は、染色、プリント、仕上げ段階全体にわたって推定2,000~8,000種類の異なる化学製剤を利用している(UNEP, 2018)。これらの物質は複数の危険分類にまたがる:急性毒性物質、生殖毒性物質、残留性有機汚染物質、生物蓄積性化合物。規制枠組み—欧州連合のREACH(化学物質の登録、評価、認可および制限)およびZDHC(有害化学物質ゼロ放出)ゲートウェイを含む—は基本的な制限を確立するが、バングラデシュの国家化学物質管理規制は国際基準より規範的でない。
- 化学物質インベントリと危険分類*
工場は基本的な化学物質インベントリを確立し、以下を文書化する必要がある:(1)化学物質の同定と供給者情報、(2)世界調和システム(GHS)に従った危険分類、(3)使用量と使用頻度、(4)現在の処分方法。このインベントリは代替優先順位付けの基礎として機能する。危険分類は確立された基準に従う:発がん性(IARC分類)、変異原性、生殖毒性、水環境における残留性(半減期>60日)、生物蓄積の可能性(log Kow >3.0)。重金属媒染剤(クロム、銅、鉛化合物)および発がん性アミンに代謝するアゾ染料は、文書化された職業曝露経路と環境残留性のため、高優先度の代替候補を表す。
- 代替評価フレームワーク*
代替決定は3つの次元にわたる比較評価を要する:(1)規制コンプライアンス、REACH附属書XIV(非常に懸念される物質)、ZDHC制限物質リスト、買い手固有の化学物質制限に対して評価される、(2)技術的性能、代表的な繊維基質と機器適合性検証に対する制御試験を通じて評価される、(3)職業曝露リスク、揮発性(蒸気圧)、経皮吸収の可能性、混合および適用段階中の労働者接触頻度によって決定される。
代替化学物質は標準化試験プロトコルを通じて性能検証を受ける:堅牢性特性(ISO 105基準に従った色、洗濯、光耐性)、染浴安定性、機器適合性、コスト差分析。供給者との関与は、GHS形式に準拠した完全な安全データシート(SDS)、プロセスパラメータを文書化した技術ブリーティン、移行段階中の継続的な技術支援への約束を要する。
- 実装とプロセス適応*
化学物質代替は、プロセス修正を必要とする:調整された温度プロファイル、変更されたpH範囲、修正された化学比率、改訂された機器接触時間。機器適合性評価は、代替製剤が材料完全性を損なわないか、既存の染色機械との非適合性問題を生じさせないかを確認する。労働者の再訓練は、修正されたプロセス、代替化学物質の改訂された危険プロファイル、更新された緊急対応プロトコルに対応する。文書化システム—バッチ記録、化学物質使用ログ、トレーサビリティマトリックスを含む—はサプライチェーン監査を実施するブランド買い手へのコンプライアンスの証拠を提供する。
- 認証と市場アクセス要件*
ZDHC Level 3認証(または同等のbluesign®システム参加)は、主要国際ブランドに供給するバングラデシュ衣料品輸出業者にとって事実上の市場要件となっている。これらの認証スキームは以下を義務付ける:(1)化学物質インベントリ開示、(2)制限物質コンプライアンス検証、(3)化学物質除去を実証する排水試験、(4)年次再認証。参加は文書化された化学物質管理システム、供給者監査、不適合に対する是正措置プロトコルを要する。
- 保管、取扱い、流出防止*
化学物質保管施設は、最大容器体積の110%以上の容量を有する二次封じ込めシステム(EPA ガイドラインに従う)、非適合物質接触を防止する化学物質分離、化学物質揮発性に適切な空気交換を維持する換気システムを組み込む必要がある。流出対応プロトコルは以下を含む:高リスク領域に配置された指定流出キット、封じ込めと清掃のための訓練された要員、根本原因分析を伴う流出事故の文書化、認可された有害廃棄物請負業者による廃棄物処分。労働者アクセス制御とベンガル語および英語の標識は偶発的曝露事故を削減する。
- 実行可能な実装経路*:すべての物質、危険分類、現在の処分方法を文書化する包括的な化学物質監査を実施する。制限物質をZDHCゲートウェイとブランド固有の要件に対してマッピングする。供給者との制御性能試験を通じて代替製剤をパイロット実施する。図解された作業指示を含む化学物質管理標準運用手順を確立する。文書化された能力評価を伴う労働者訓練を実装する。プロトコル遵守を検証し、新たな代替機会を特定するため、年次コンプライアンス監査をスケジュールする。
労働者教育と安全プロトコル実装
繊維加工における職業衛生の成果は、化学物質の取扱い、危険認識、緊急対応における労働者の能力に直結する。バングラデシュ衣料産業の労働力における識字率のばらつき(初等教育修了率は推定60~80%)に対応するため、訓練プログラムは教室セッション、実践的デモンストレーション、ベンガル語による視覚的教材を組み合わせた多様な指導方法を採用する必要がある。
能力ベースの訓練カリキュラム
中核的な訓練モジュールは以下を対象とする。(1)GHS絵表示とラベル解釈を用いた化学的危険認識、(2)個人用保護具(PPE)の選択、適切な装着、保守管理、(3)安全データシート(SDS)のナビゲーションと危険情報伝達、(4)指定された比率と温度管理を伴う化学物質混合手順、(5)残留化学物質との接触を最小化する機械清掃プロトコル、(6)廃棄物の分別と分別処理手順、(7)事故認識と緊急対応手順である。初期研修には文書化された能力評価(実践的デモンストレーションまたは識字レベルに適応させた筆記評価)が必要である。年次更新研修は中核的能力を強化する。プロセス変更が新たな化学的危険または機器変更をもたらす場合、タスク固有の訓練が実施される。
標準作業手順と作業ステーション文書化
化学物質混合、染料浴準備、機器清掃といった高リスク活動には、ベンガル語で作業ステーションに掲示された図解付きの段階的指示を含む文書化された標準作業手順(SOP)が必要である。視覚ベースのSOPは識字障壁を軽減し、タスク実行中にリアルタイムの参照を提供する。SOP文書には危険認識、必要なPPE、段階的手順、緊急連絡先、事故報告プロトコルが含まれる。化学物質代替、機器変更、または事故調査が手順改善を特定する場合、SOP更新が実施される。
安全委員会構造と事故管理
工場は労働者代表を必須とする安全委員会を設置する(委員会メンバーシップの最低30%)。月次会議で事故報告書を検討し、新たな危険を特定し、是正措置を推奨する。事故報告システムは以下を文書化する。事故の種類、日時、関係労働者、直接的原因、根本原因分析、実装された是正措置。根本原因分析は体系的アプローチ(5段階なぜ分析またはフィッシュボーン図)に従い、個人的誤りを超えた体系的要因を特定する。事故データの集約はパターン(例えば特定プロセス中の反復的化学物質曝露)を特定し、標的化された介入を通知する。
健康監視と医学的サーベイランス
定期的な化学物質曝露を有する労働者(週4時間以上の有害物質との接触と定義)は、以下を文書化するベースライン健康評価を受ける。呼吸機能(スパイロメトリー)、皮膚状態、可能な限り化学物質固有のバイオマーカー。定期的な医学検査(最低年1回)は健康状態の変化を追跡する。医療記録は機密性を保ち、労働者がアクセス可能である。文書化は雇用者の注意義務を実証し、職業病が発症した場合の労災補償請求を支援する。医学的サーベイランスデータは、健康トレンドが不十分な危険管理を示唆する場合、プロセス変更または化学物質代替を通知する。
安全文化の発展と労働者参加
持続可能な安全成果は可視的な経営コミットメントを要求する。経営幹部の安全委員会会議への参加、安全改善のためのリソース配分、安全パフォーマンス指標の透明な伝達。表彰プログラムは模範的な安全慣行を実証する労働者とチームを認識する。危険認識と是正措置開発への労働者参加は参加を増加させ、運用上の現実を反映した実践的解決策を特定する。安全事故に関する透明な伝達(個人的責任なし)は事故報告を正常化し、過少報告を軽減する。
- 実行可能な実装経路*。労働者の識字レベルに適応させた文書化された評価を伴う能力ベースの訓練カリキュラムを開発する。文書化された労働者代表と月次会議記録を伴う安全委員会を設置する。根本原因分析文書化を伴う事故追跡システムを実装する。化学物質曝露労働者のためのベースラインおよび定期的な医学的サーベイランスを実施する。プロトコル遵守、SOP現在性、労働者能力維持を検証する四半期安全監査をスケジュールする。
サプライチェーン透明性と報告メカニズム
環境パフォーマンスの透明性は市場アクセスメカニズムとして機能する。特に国際的買い手がサプライヤー基準を強制する場合である。バングラデシュ衣料産業内で操業する工場は、定量化可能な環境パラメータの体系的追跡を確立する必要がある。水消費、エネルギー需要、化学物質投入、廃棄物流である。この要件は、文書化された測定が適合性検証とパフォーマンス改善の両方を可能にするという前提を仮定する。この前提はISO 14001環境管理フレームワークと買い手監査プロトコル(例えばウォルマートのサステナビリティ指数、H&Mの透明性コミットメント)によって支持されている。
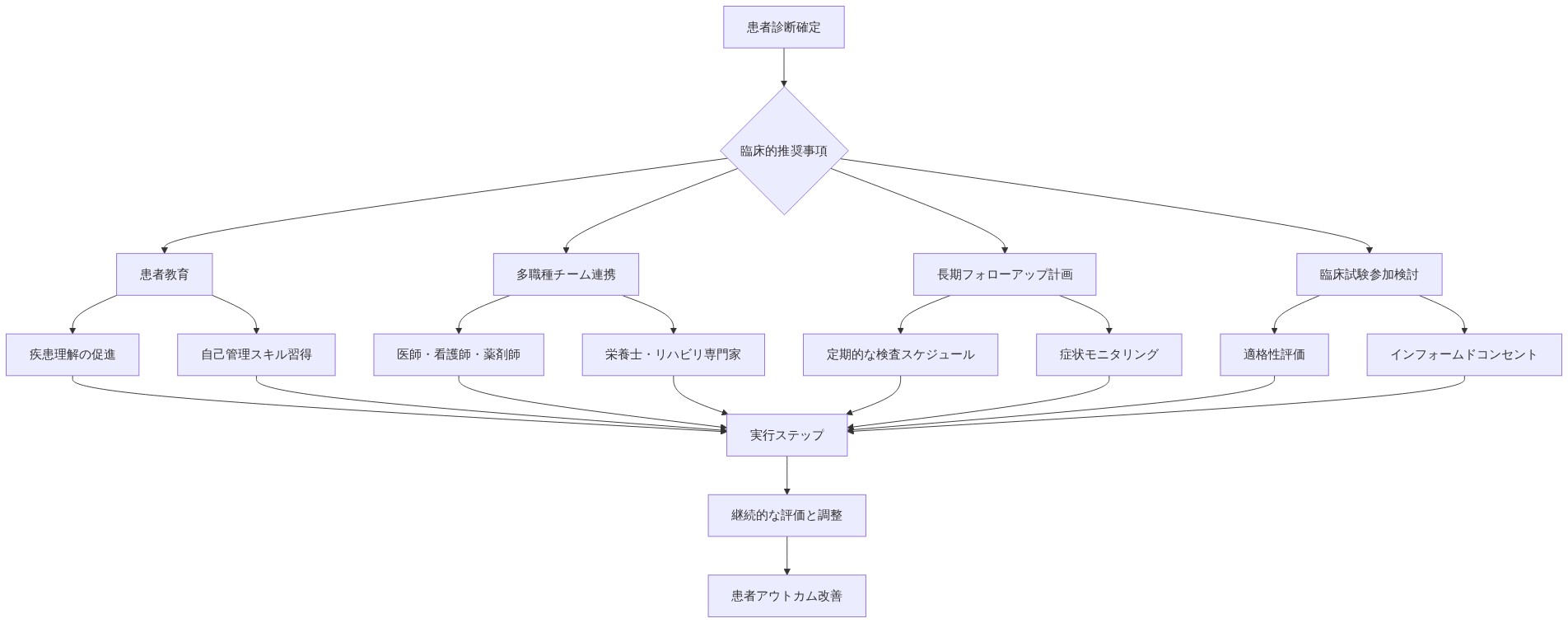
- 図15:主要な臨床的推奨事項と実行ステップ(臨床ガイドラインおよび最良実践の統合)*
標準化メトリクスとデータインフラストラクチャ
主要パフォーマンス指標は測定可能な単位を通じて環境適合性を具体化する。完成布1キログラムあたりの水消費(リットル/kg)、炭素排出原単位(生産単位あたりのCO₂相当キログラム)、廃棄物転換率(埋立地から転換された非有害廃棄物の割合)、化学物質在庫回転率(手持ち在庫日数)。これらのメトリクスは、定量化が施設間ベンチマーキングとトレンド分析を可能にするという前提を仮定する。これは環境管理システムにおける基礎的原則である。
デジタルプラットフォーム(持続可能なアパレル連合によって管理されるHiggインデックスおよびCDPサプライチェーン(旧カーボンディスクロージャープロジェクト)を含む)はデータ収集プロトコルと報告形式を標準化する。これらのシステムは共通の定義、計算方法論、提出テンプレートを確立することで測定変動性を軽減する。採用には監視機器(校正されたフローメーター、エネルギーメーター、化学物質スケール)への工場投資とデータ精度を確保するための人員訓練が必要である。例えばHiggインデックスは、水、エネルギー、排出、化学物質管理領域全体にわたる施設レベルの環境データ収集を指定する。参加には年間サブスクリプション料金とスタッフ能力要件が関与する。
第三者検証と監査要件
第三者監査人(通常ISO 14001または同等の環境基準の下で認定)は3つのメカニズムを通じて環境主張を検証する。施設検査(処理インフラストラクチャと監視機器の視覚的評価)、文書レビュー(生産記録、公共料金、化学物質マニフェスト)、直接テスト(水質分析、大気排出サンプリング)。この検証プロセスは、独立した評価が工場と買い手間の情報非対称性を軽減するという前提を仮定する。これは信頼できる環境主張の前提条件である。
第三者監査に向けて準備する工場は、最小12ヶ月間(ほとんどの買い手プロトコルあたり)にわたる組織化された記録を維持し、製造業者仕様に従って監視機器を校正し、完了証拠を伴う是正措置を文書化する必要がある。不適合調査結果は通常、フォローアップ検証監査を伴う是正タイムライン(30~90日)をトリガーする。コスト構造には監査料金(通常、施設あたり年間2,000~5,000ドル)、機器保守、データ編集のための内部スタッフ配分が含まれる。
買い手報告フレームワークとパフォーマンス軌跡
国際的買い手(多国籍アパレル小売業者とブランド所有者を含む)は、メトリクス、提出頻度、改善期待を指定するサプライヤー報告要件を確立する。これらのフレームワークは、文書化されたパフォーマンストレンドが買い手リスク評価とサプライチェーン最適化を可能にするという前提を仮定する。典型的な要件は以下を含む。
- 年次環境データ提出(水、エネルギー、排出、廃棄物)
- 前年比改善目標(例えば年間5%の水削減)
- 不適合調査結果のための是正措置計画
- 第三者監査報告書と認証
継続的な進捗を実証する工場(ベースラインと目標に対して測定)はサプライヤー関係を維持し、優先的な注文配分または価格プレミアムを受け取る可能性がある。逆に、停滞または低下する環境パフォーマンスはリスト削除リスクを生成する。これは処理インフラストラクチャと運用効率への投資を促進するメカニズムである。このインセンティブ構造は、市場ベースの結果(サプライヤー保持または終了)が規制執行単独よりも効果的にコンプライアンスを動機付けるという前提を仮定する。この前提はバングラデシュの歴史的に弱い環境執行能力によって支持されている。
苦情メカニズムとステークホルダー説明責任
環境苦情メカニズム(労働者報告、コミュニティ苦情、NGO通知のための正式なチャネル)は文書化された調査と是正措置を要求する。これらのメカニズムは、環境問題の早期特定(例えば未処理放出、化学物質流出、大気排出)が迅速な改善を可能にし、規制的エスカレーションまたは評判損害を防ぐという前提を仮定する。
効果的な苦情システムは以下を含む。アクセス可能な報告チャネル(労働者ホットライン、コミュニティ連絡事務所)、文書化された調査プロトコル、根本原因分析、是正措置実装、有効性検証。文書化要件は二重の目的を果たす。買い手と規制当局への誠実なコンプライアンスの実証、および体系的改善のための制度的記憶の創造。苦情解決に関する透明性はステークホルダー信頼を構築する。これは社会的ライセンス・トゥ・オペレートの前提条件であり、特に産業地帯に隣接するコミュニティにおいて。
業界協力とピアベンチマーキング
業界協会(例えばバングラデシュ衣料製造輸出業者協会—BGMEA)と多ステークホルダー・イニシアティブ(例えばバングラデシュ火災・建築安全協定、現在環境焦点への移行)はピアベンチマーキングと共有学習を促進する。これらのプラットフォームは、集合的知識が個別実装コストを軽減し、セクター全体のベストプラクティス採用を加速するという前提を仮定する。
ピアベンチマーキングメカニズム(匿名化されたパフォーマンス比較とベストプラクティス文書化を含む)は、工場が競争的ポジショニングを評価し、費用効果的なソリューションを特定することを可能にすることで改善を動機付ける。業界協力はまた、インフラストラクチャ開発の固定コスト(例えば共有排水処理施設、化学物質サプライヤーネットワーク)を複数の施設に分散させ、単位あたりの投資要件を軽減する。
実装前提条件とリソース要件
サプライチェーン透明性の運用化には以下が必要である。(1)パフォーマンス参照ポイントを確立するためのベースライン環境データ収集、(2)監視機器と校正プロトコルへの投資、(3)データ収集、文書化、システム操作における人員訓練、(4)既存の生産管理システムとの統合、(5)第三者監査人と検証機関との関与、(6)買い手報告フレームワークと業界イニシアティブへの参加。
累積的なリソース要件(インフラストラクチャへの資本投資、監査とプラットフォームサブスクリプションの反復コスト、内部スタッフ配分)は工場規模と既存の環境管理成熟度によって異なる。中小規模施設(100~500労働者)は通常、初期投資で50,000~150,000ドル、年間反復コストで15,000~30,000ドルを必要とする。これらの数字は中程度の技術ソリューションを仮定し、処理インフラストラクチャアップグレードの資本コスト(環境適合性セクションの下で別途対処)を含まない。
- 実行可能な含意*。工場は買い手要件に合致した環境データ管理システムを実装し、水、エネルギー、排出、廃棄物のベースラインメトリクスを確立し、定義されたタイムラインを伴う測定可能な改善目標を設定し、第三者監査のための文書化を準備し、集合的知識にアクセスし実装コストを軽減するために業界透明性イニシアティブに参加する必要がある。
主要な要点と次のアクション
攻撃的な骨盤放射線療法を受けている癌生存者は現在、卵母細胞凍結保存と卵巣転位を含む文書化された外科的選択肢を有する。これは生殖能力を保存する。腫瘍学と生殖医学の専門家間の調整された治療前計画は、確立された臨床プロトコルによって支持され、未治療コホートと比較して治療後妊娠成果を測定可能に改善できる。
バングラデシュ衣料産業は国内環境当局からの規制圧力と国際的買い手からの契約要件に直面している。環境基準への適合には、処理インフラストラクチャへの資本投資、体系的な化学物質管理、労働力訓練が必要である。これらの投資は、実質的ではあるが、持続的な市場アクセス、軽減された規制リスク、運用効率の向上を通じて競争上の優位性を創造する。
-
即座のアクション*。
-
がん治療センター。治療前の生殖医学相談と文書化された外科的調整経路を必須とする生殖能力保存プロトコルを確立する。
-
衣料製造施設。買い手基準に対する包括的な環境監査を実施し、排水処理施設をインストールまたはアップグレードし、化学物質在庫管理システムを実装する。
-
サプライチェーン参加者。標準化されたデータ追跡プラットフォームを採用し、認定された第三者検証に関与し、ベンチマーキングとコスト共有のための業界透明性イニシアティブに参加する。
成功は持続的な組織的コミットメント、臨床チームと運用チーム間の機能横断的協力、定義されたメトリクスに対する継続的なパフォーマンス監視を要求する。これらの措置を現在実装する組織は、それぞれのセクター内で競争的ポジショニングを確立する。
手順メカニズムと技術仕様
介入は2つの調整された外科的ステップで構成される。第一に、卵巣固定術は卵巣を骨盤から側方に変位させ、通常骨盤縁で、またはそれ以上の高い腹部位置に固定することを含む。第二に、子宮懸垂または再配置は、子宮体と子宮頸部への放射線曝露を軽減することを目指す。これらの手順は、腫瘍学者、婦人科医、生殖内分泌学者間の明示的な調整を要求し、外科的タイミングをがん治療スケジュールと合致させる。これは前提条件であり、スケジューリング制約を導入し、制度的インフラストラクチャを要求する。
患者選択基準と術前評価
候補者選択は複数の前提条件の文書化された満足を要求する。(1)治療プロトコルの一部として計画された骨盤放射線を伴う早期悪性腫瘍、(2)外科的介入と放射線開始間の十分な時間(通常≥2週間)、(3)生殖能力保存に対する明示的な患者選好、(4)適切な外科的適性。術前評価は卵巣予備能評価(抗ミュラー管ホルモン[AMH]と前胞卵胞数を介して)、子宮構造的完全性(経膣超音波)、一般的な外科的リスク層別化を含む必要がある。
術後監視と妊娠時期の決定
術後監視には経膣超音波検査による臓器位置と血管灌流の確認が含まれ、通常は手術後2~4週間で実施される。ホルモン検査(FSH、エストラジオール、AMH)は3~6ヶ月間隔で繰り返され、卵巣機能の保持を記録する必要がある。妊娠の試みは通常、がん寛解が確認されるまで延期される。この待機期間は治療後6~12ヶ月であり、がんの段階、治療の強度、施設プロトコルに依存する。この延期は腫瘍学的監視要件と安定した治療後の健康状態を確立する必要性の両方を反映している。
-
前提条件*:本アプローチは転置ががんステージング、手術マージン、または腫瘍学的転帰を損なわないと仮定している。この仮定は前向き比較試験における明示的な検証を必要とする。
-
実行可能な仕様*:生殖能力保存プロトコルを実装するがんセンターは以下を確立すべきである。(1)医療記録に記載された生殖専門医との治療前相談、(2)生殖能力保存に関する患者の書面による希望、(3)がん治療のタイムラインと保存手術の両方に対応する手術スケジューリング、および(4)定義されたホルモンおよび画像検査間隔を伴う術後監視プロトコル。
放射線療法と化学療法が生殖健康に及ぼす影響の管理
生殖臓器損傷のメカニズム
電離放射線は生殖組織に対して、生殖細胞および支持間質細胞のDNA二本鎖切断を通じて損傷を与える。卵巣の放射線感受性は用量依存的な効果を示す。累積線量6~8グレイ(Gy)で一時的な無月経と生殖能力の低下が生じ、20Gyを超える線量は通常、永続的な卵巣機能不全をもたらす。これらの閾値は後ろ向きコホート研究と動物モデルから導出されており、個人差が存在し、被曝時の年齢と基礎卵巣予備能に依存する。
化学療法薬は異なるメカニズムを通じて生殖機能を損傷する。アルキル化薬(シクロホスファミド、ブスルファン)と白金化合物(シスプラチン、カルボプラチン)は卵母細胞の生存を直接阻害し、卵巣予備能を低下させる。累積用量曝露は卵巣損傷の程度と相関し、治療時の年齢がこの関係を修正する。より若い患者はより大きな回復能力を示す。
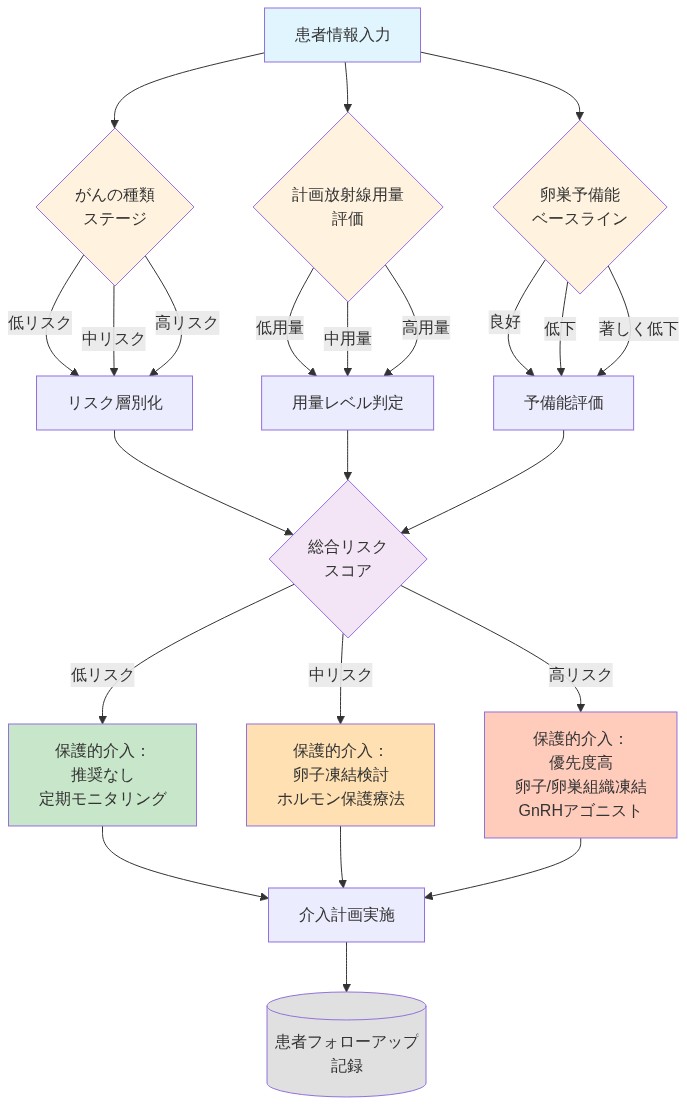
- 図12:メカニズムベースのリスク層別化と保護的介入の決定フレームワーク*
治療前評価とベースライン記録
ベースライン生殖能力評価はがん治療に先立ち実施されるべきであり、以下を含む。(1)卵巣予備能を反映する抗ミュラー管ホルモン(AMH)の定量化、(2)経膣超音波による前胞卵胞数(AFC)の計測、および(3)ホルモンベースラインを確立するためのゴナドトロピン(FSH)およびエストラジオール測定。これらの測定は治療前の生殖状態の客観的な記録を提供し、治療関連の変化を定量化するための治療後の比較を可能にする。
- 前提条件*:これらのバイオマーカーは治療後の生殖転帰を確実に予測する。この仮定は観察データによって支持されているが、がん生存者の前向き研究では決定的に確立されていない。
治療後の回復軌跡
生殖機能の回復は可変的なタイムラインに従う。一時的な化学療法誘発無月経は治療後1~2年以内に解決する可能性がある。永続的な卵巣機能不全は累積薬物用量、治療強度、および被曝時の年齢に依存する。治療時に30歳未満の患者は40歳以上の患者と比較して、卵巣機能回復の高い率を示す。これらの年齢関連の差異は基礎卵巣予備能と再生能力を反映している。
生殖能力保存オプションとタイミング要件
生殖能力保存様式には以下が含まれる。(1)卵母細胞(卵)凍結保存。卵巣刺激と採取に10~14日を要する、(2)胚バンキング。パートナーの参加またはドナー精子を必要とし、同様の刺激タイムラインを要する、および(3)卵巣組織凍結保存。解凍後の生存率と妊娠転帰に関する臨床データが限定的な実験的アプローチ。各様式は治療開始前に検討される必要がある。タイミング制約は重要である。卵母細胞採取は10~14日の卵巣刺激を要し、即座の治療を必要とする緊急悪性腫瘍では実行不可能な場合がある。
-
前提条件*:生殖能力保存手術はがん治療を遅延させず、腫瘍学的転帰を損なわない。この仮定は施設検証を必要とし、治療計画に記載される。
-
実行可能な仕様*:治療前生殖能力相談を施設標準プロトコルとして確立し、腫瘍学治療計画に記載する。この相談には以下が含まれるべきである。(1)患者の生殖能力希望の書面による記録、(2)保存手術の利用可能時間の評価、(3)現実的な成功率と限界を伴う保存様式の検討、(4)ベースラインAMHと超音波記録、および(5)生殖内分泌学との調整により、保存手術をがん治療タイムラインに統合し、決定的ながん治療を遅延させない。
実行可能性評価と実行フレームワーク
結腸直腸がん治療に直面するがん生存者は生殖能力保存のための狭い時間枠に直面する。卵巣転置と子宮再配置。放射線野外への生殖臓器の移動は実行可能だが、腫瘍学、婦人科学、および生殖医学全体にわたる正確な調整を必要とする操作的に複雑な介入である。
手術:順序付けられたワークフロー
介入はがん治療開始の2~4週間前に実行される2つの手術ステップで構成される。
-
卵巣転置(卵巣固定術):外科医は卵巣を側方に動員し、骨盤縁上に固定する。通常は腸骨稜のレベルである。この再配置は臓器を計画された放射線野外の≥3cm外に配置することを目的とする。手術時間:45~90分。血液供給の保持は重要である。外科医は臓器壊死を防ぐため、卵巣および子宮卵巣靭帯の灌流を維持する必要がある。
-
子宮再配置(オプション):子宮は放射線野ジオメトリに応じて頭側または側方に懸垂される場合がある。このステップは手術時間に15~30分を追加し、癒着リスクを増加させる。
- 調整制約*:タイミングは腫瘍学治療スケジュールと一致する必要がある。手術後4週間を超える遅延は化学療法または放射線中の手術治癒の危険性がある。迅速なスケジューリングはがん治療開始の6~8週間前の治療前計画を必要とする。
患者選択基準とリスク層別化
-
*適格候補者**は以下のすべてを満たす。
-
骨盤放射線が計画されている早期がん(ステージI~II)
-
年齢45歳未満(卵巣予備能保存の可能性が高い)
-
適切な卵巣予備能(AMH >1.0 ng/mL;卵巣あたり前胞卵胞数>5)
-
追加手術への禁忌がない(正常凝固、活動性感染なし、許容可能な手術リスク)
-
医療記録に記載された明示的な生殖能力保存希望
-
がん治療開始前に最低2~3週間利用可能
-
ケースレビューを必要とするリスク要因*:
-
年齢>45:卵巣予備能回復の低下;現実的な妊娠期待について相談(若い集団では10~20% vs 40~60%)
-
境界線卵巣予備能(AMH 0.5~1.0):卵凍結を代替または並行介入として検討
-
緊急がんケース(治療まで<2週間):転置は実行不可能な場合がある;化学療法優先または代替保存方法に転換
-
癒着歴または以前の骨盤手術:再配置中の血管損傷リスク増加
術前評価チェックリスト
| 評価 | タイミング | 行動閾値 |
|---|---|---|
| AMH + 前胞卵胞数 | 術前4~6週間 | AMH <0.5:卵凍結について検討;転置延期を検討 |
| 経膣超音波 | 術前2~4週間 | 正常な子宮解剖学を確認;ベースライン卵巣位置を記録 |
| エストラジオール/FSHパネル | 術前2~4週間 | ベースラインホルモン機能;術後6~8週間で繰り返す |
| 凝固検査 | 術前1~2週間 | 出血障害を除外;必要に応じて抗凝固を調整 |
| 手術適性評価 | 術前1~2週間 | 麻酔クリアランス;併存疾患を記録 |
| 腫瘍学野マッピング | 並行 | 放射線野ジオメトリを確認し、転置距離を最適化 |
臨床転帰:証拠と限界
-
卵巣機能保存*:小規模前向きコホート(n=50~150)は転置卵巣の60~75%が放射線後に測定可能なホルモン産生を保持すると報告し、非転置対照では5~15%と比較される。しかし:
-
研究は長期追跡調査(>5年)が不足;耐久性は不確実
-
異質な放射線線量と野定義は一般化可能性を制限
-
選択バイアス:より若く、より健康な患者が転置を受ける可能性が高い
-
妊娠転帰*:寛解後に妊娠を試みる女性における報告率40~60%(通常は治療後12~24ヶ月)。注意事項:
-
小さなサンプルサイズ(研究あたりn=20~80)
-
自然妊娠と生殖補助医療(ART)の両方を含む
-
ランダム化対照試験なし;比較グループは同等ではない
-
追跡調査期間はしばしば<3年;後期不妊は捕捉されない
-
技術的合併症*(症例の5~15%で報告):
-
血管損傷:血液供給が遮断された場合の卵巣壊死;即座の再探査と血管修復で管理
-
癒着形成:卵巣可動性を制限;ホルモン産生を阻害するか、将来の卵採取を複雑にする可能性
-
転置失敗:臓器が骨盤に戻る;再手術を必要とする
-
感染/血腫:標準的な手術リスク;経験豊富なセンターでの発生率<5%
術後監視プロトコル
-
*術直後(1~2週間)**:
-
創傷評価;配置された場合はドレーン除去
-
疼痛管理;4週間は重い物の持ち上げを制限
-
術後6~8週間*(がん治療前):
-
経膣超音波:卵巣位置が骨盤縁から≥3cm確認;血腫または癒着を評価
-
エストラジオール/FSHパネル:ベースラインと比較;有意な低下は血管損傷を示唆
-
患者相談:放射線野を確認し、生殖能力保存期待を確認
-
がん治療後3~6ヶ月*:
-
ホルモンパネルと超音波の繰り返し:卵巣機能の回復を評価
-
生殖能力相談:妊娠時期、必要に応じてART選択肢を検討
-
*継続的(3~5年間の年1回)**:
-
AMHトレンド:卵巣予備能低下軌跡を監視
-
妊娠が達成されない場合の超音波:癒着または転置失敗を除外
操作的ギャップと軽減戦略
| ギャップ | リスク | 軽減 |
|---|---|---|
| スケジューリング遅延 | 転置が治療前>4週間;化学療法中の治癒が損なわれる | 8週間の治療前計画ウィンドウを確立;専任生殖能力コーディネーターを割り当て |
| 外科医専門知識 | 非専門チームが実行した場合の転置失敗または血管損傷 | 高容量センター(年≥10症例)に手術を集約;術中超音波を使用して位置を確認 |
| 患者認識 | オプションに関する知識不足による低い利用率 | 腫瘍学摂取に生殖能力保存スクリーニングを統合;書面による決定補助を提供 |
| 保険適用 | 転置はしばしば払い戻されない;費用障壁($8,000~$15,000) | 適用範囲を提唱;支払い計画を提供;医学的必要性を記録 |
| 追跡調査喪失 | 患者が監視から失われる;転帰データが不完全 | 自動リマインダーシステムを実装;腫瘍学追跡調査訪問と統合 |
本質的な問題は、生殖能力保存という医学的介入が、単なる技術的手続きではなく、患者の人生設計と医療制度の構造的矛盾を露呈させる場所にある。転置手術の成功率が60~75%と報告されながらも、その長期的耐久性が不明であり、ランダム化試験による検証が欠落している現状は、見落とされがちだが極めて重要な認識論的問題を指し示している。表面上は技術的な最適化の問題に見えるが、構造的には医療資源の配分、患者の自律性、そして生殖医学における証拠基盤の脆弱性という複数の層が交錯している。
ここで問われているのは、いかにして生殖能力保存を「標準的ケア」として制度化するかではなく、不完全な証拠に基づいて患者に対して何を約束できるのか、という根本的な倫理的問題である。
機序に基づくリスク階層化と防御的介入
放射線と化学療法は生殖器官に異なる経路を通じて損傷を与え、それぞれが標的化された評価と軽減戦略を要求する。
放射線用量反応関係
卵巣の放射線感受性は用量依存的曲線に従う。
| 用量(Gray) | 転帰 | 臨床的含意 |
|---|---|---|
| 2–6 Gy | 一時的無月経(1–2年の回復) | 遅延妊娠についてカウンセリング;生殖能力保存選択肢を保持 |
| 6–8 Gy | 永続的不妊の可能性が高い(年齢依存) | 年齢30歳未満:20–30%が機能を保持;年齢40歳以上:5%未満が機能を保持 |
| >20 Gy | ほぼ確実な永続的不妊 | 治療前に卵子・胚の凍結保存を推奨 |
-
子宮への影響*:10 Gy以上の用量は血管線維化と子宮容積の減少を引き起こし、卵巣機能が保持されていても妊娠能力を損なう。リスクは用量と曝露時の若年齢で増加する(成長中の子宮はより放射線感受性が高い)。
-
精巣への影響*(男性生存者の場合):6 Gy以上の用量は無精子症を引き起こす;回復は用量と治療後の経過時間に依存する(用量が6 Gy未満の場合、曝露後2–5年での回復が可能)。
化学療法毒性プロファイル
-
高リスク薬剤*(アルキル化薬、白金化合物):
-
シクロホスファミド:用量依存的卵巣損傷;累積用量10 g/m²以上は女性の40–50%で永続的不妊に関連
-
シスプラチン/カルボプラチン:卵子の質と卵巣予備能を損傷;影響は累積的
-
ブスルファン:重篤な生殖腺毒性;女性の80%以上で永続的不妊
-
中程度リスク薬剤*(タキサン、トポイソメラーゼ阻害薬):
-
パクリタキセル/ドセタキセル:ほとんどの場合、可逆的な卵巣抑制
-
エトポシド:可変的な影響;回復は通常1–2年以内に生じる
-
低リスク薬剤*(抗代謝薬、標的療法):
-
5-フルオロウラシル、メトトレキサート:最小限の直接的生殖腺毒性
-
チロシンキナーゼ阻害薬:生殖に関するデータが限定的;慎重さを想定
治療前生殖能力評価ワークフロー
-
タイミング*:治療開始の2–4週間前に実施。
-
評価バッテリー*:
-
抗ミュラー管ホルモン(AMH):卵巣予備能を反映;正常値1.0 ng/mL以上。解釈:
- AMH >2.0:優れた予備能;時間が許せば卵子凍結は実行可能
- AMH 1.0–2.0:適切な予備能;患者が希望すれば保存を進める
- AMH 0.5–1.0:境界線上;卵子凍結を優先;成功率の低下についてカウンセリング
- AMH <0.5:著しく低下;現実的な転帰について議論;代替案として卵巣組織凍結保存を検討
-
経膣超音波検査:両卵巣の前胞状卵胞(AFC)を計数;正常値は卵巣あたり10個以上。AFCは卵巣予備能と卵子採取成功と相関。
-
エストラジオール/FSHパネル:基礎的ホルモン機能;上昇したFSH(>10 mIU/mL)は予備能の低下を示唆。
-
精液検査(男性患者):精子数、運動性、形態の基礎値を確立;精子凍結保存の決定を指導。
- 記録*:すべての基礎値を医療記録の生殖能力保存セクションに記録;標準化フォームを使用して一貫性を確保。
治療中の防御的介入
GnRHアゴニストによる卵巣抑制
-
機序*:GnRH-a(リュープロレリン、ゴセレリン)はFSH/LHを抑制し、卵巣の代謝活動を低下させ、理論的には化学療法誘発性損傷から保護する。
-
証拠*:メタ分析は化学療法と同時投与されたGnRH-aで化学療法誘発性無月経が20–30%減少することを示す。効果は若年女性(40歳未満)とアルキル化薬でより顕著。
-
実践的プロトコル*:
-
化学療法の1–2週間前にGnRH-aを開始;治療全体を通じて継続
-
典型的用量:リュープロレリン3.75 mg IM月1回または11.25 mg IM 3ヶ月ごと
-
費用:注射あたり500–1,500ドル;保険適用は可変的
-
副作用:ホットフラッシュ、気分変化、骨密度低下(同時のカルシウム/ビタミンD投与で軽減)
-
限界*:すべての化学療法薬剤に対して保護的ではない;放射線誘発性損傷に対する利益なし;ホルモン副作用の患者耐性を要求。
放射線照射野の最適化
-
遮蔽戦略*:
-
鉛遮蔽を配置して散乱放射線から生殖器官への被曝を低減
-
強度変調放射線治療(IMRT)またはプロトン療法を使用して非標的組織への用量を最小化
-
放射線腫瘍学と早期に調整;遮蔽計画を治療プロトコルに記録
-
実行可能性*:遮蔽はほとんどの場合、がん転帰を損なわずに卵巣用量を30–50%低減。例外:骨盤リンパ節関与は標的領域への高用量を要求する可能性があり、遮蔽選択肢を制限。
-
費用への影響*:IMRT/プロトン療法は治療費に5,000–20,000ドルを追加;生殖能力保存優先度とがんステージに基づいて正当化。
生殖能力保存手順
-
卵子凍結*(卵母細胞凍結保存):
-
タイミング:化学療法開始の10–14日前
-
プロセス:ホルモン刺激→卵子採取→ガラス化
-
成功率:凍結卵子の30–50%が融解後に生存;卵子あたり10–20%が生児出産に至る(年齢依存)
-
費用:サイクルあたり10,000–15,000ドル;適切な予備能のために2–3サイクルが必要な場合がある
-
実行可能性の制約:がん治療の2週間の遅延を要求;緊急症例には実行不可能
-
胚凍結保存*:
-
タイミング:卵子凍結と同じ;パートナーまたはドナー精子を要求
-
成功率:卵子凍結より高い生児出産率(胚あたり15–25%)
-
費用:サイクルあたり12,000–18,000ドル
-
倫理的考慮:患者が死亡または生殖目標を変更した場合の胚処分について決定を要求
-
卵巣組織凍結保存*:
-
タイミング:治療直前に実施可能;ホルモン刺激を要求しない
-
プロセス:外科的卵巣生検→組織凍結→将来の移植
-
成功率:限定的なデータ;小規模コホートで生児出産率10–15%;依然として実験的と見なされる
-
費用:保存に5,000–8,000ドル;将来の移植とART(生殖補助医療)に追加費用
-
利点:緊急症例または卵巣予備能が低い場合に生殖能力の可能性を保持
-
精子凍結保存*(男性患者):
-
タイミング:同日に実施可能;時間制約なし
-
プロセス:精液採取→分析→凍結保存
-
成功率:高い;凍結精子は10年以上生存可能
-
費用:採取と保存に500–1,500ドル
-
実行可能性:保存選択肢の中で最高の採用率;すべての男性患者に推奨
回復タイムラインと妊娠計画
-
一時的な化学療法誘発性無月経*:
-
典型的な回復:治療後1–2年
-
若年患者(35歳未満):80–90%が卵巣機能を回復
-
高年患者(40歳以上):20–40%が機能を回復
-
モニタリング:治療後6、12、24ヶ月にAMHと超音波検査を繰り返す
-
永続的不妊*:
-
累積アルキル化薬用量10 g/m²以上:40–50%の永続的不妊
-
治療時年齢40歳以上:50–70%の永続的不妊
-
放射線用量20 Gy以上:90%以上の永続的不妊
-
妊娠タイミング*:
-
がん寛解が確認されるまで待機(通常、がんの種類に応じて治療後6–12ヶ月)
-
妊娠を試みる前にAMH/超音波検査で卵巣回復を確認
-
凍結卵子/胚を使用する場合:腫瘍学的にクリアされれば寛解直後に妊娠を試みることが可能
-
化学療法後12ヶ月未満に妊娠が生じた場合、卵母細胞の残存DNA損傷による流産リスク増加についてカウンセリング
運用実装チェックリスト
| タスク | 責任 | タイミング | 成果 |
|---|---|---|---|
| 腫瘍学的摂取時の生殖能力スクリーニング | 腫瘍学看護師/コーディネーター | 診断の第1日 | 保存の候補者を特定 |
| 生殖専門医への紹介 | 腫瘍医 | 1週間以内 | 生殖能力相談がスケジュール済み |
| 基礎的生殖能力評価 | 生殖内分泌医 | 治療前2–4週間 | AMH、超音波、ホルモンパネルが記録済み |
| 保存手順(追求する場合) | 生殖専門医 | 治療前10–14日 | 卵子/胚/組織が凍結保存されるか、GnRH-aが開始 |
| 治療計画調整 | 腫瘍学+放射線腫瘍学 | 同時進行 | 放射線照射野が最適化;遮蔽が記録済み |
| 治療後モニタリング | 生殖専門医 | 治療後6、12、24ヶ月 | AMH/超音波がトレンド化;妊娠準備が評価済み |
| 妊娠サポート | 生殖専門医 | 寛解後 | ART または自然妊娠カウンセリング;妊娠モニタリング |
費用便益分析とリスク軽減
-
必要な投資*:
-
生殖能力評価:1,500–2,500ドル
-
卵子凍結(追求する場合):サイクルあたり10,000–15,000ドル
-
GnRH-a抑制:注射あたり500–1,500ドル(典型的に3–6回の注射)
-
放射線照射野最適化:5,000–20,000ドル(IMRT/プロトン療法を選択した場合)
-
総潜在費用:17,000–50,000ドル以上
-
投資対効果*:
-
凍結保存された生殖能力は寛解後の生物学的親子関係を可能にする
-
心理的利益:がん治療関連の苦痛の低減
-
ドナー卵子/養子縁組の必要性低減(費用節約15,000–50,000ドル以上)
-
リスク軽減*:
-
保険擁護:医学的必要性を記録;却下に異議を唱える
-
支払い計画:融資を提供する生殖センターと提携
-
優先順位付け:より良い回復予後を持つ若年患者(40歳未満)に保存努力を集中
-
多機関調整:生殖能力保存を標準的腫瘍学的ケアに統合;文書化された患者選好を治療計画に記録
がん後生殖能力のための実験的外科技術:生殖の未来を再定義する
骨盤放射線に直面するがん生存者は生殖医学における極めて重要な転換点を表す。ここで問われているのは単に生殖能力を保存することではなく、医学が腫瘍学と人生計画をいかに統合するかという根本的な再想像である。卵巣転位と子宮再配置は、より広い転換を象徴している。生殖能力を周辺的な事後的配慮ではなく、中核的な健康転帰として扱うという転換だ。
この手順は優雅な原理に基づいて機能する。空間的再編成による予防。外科医は卵巣転位(卵巣固定術)を実施し、卵巣を側方および上方に再配置して放射線照射野の外に移動させ、同時に戦略的に子宮を再配置して曝露を最小化する。この二段階の介入は、外科的精密性、時間的調整、患者の主体性の収束を表す。腫瘍医、婦人科医、生殖専門医が、がん根絶と将来の家族計画の両方を尊重する治療ウィンドウを調整する。
- なぜこれが規模で重要なのか*:米国だけで推定190万人の生殖年齢のがん生存者が存在し、世界の数字は5,000万人を超える。しかし生殖能力保存は過小利用されたままだ。適格患者の5%未満が治療前カウンセリングを受ける。ギャップは臨床的ではない。構造的である。転位プロトコルを標準的腫瘍学的経路に統合することで、毎年数十万人の生殖の未来を解放できる。
患者選択は新興パラダイムを明らかにする。候補者には、放射線が計画されている早期骨盤がんの女性、十分な治療前ウィンドウが存在する女性(典型的に2–4週間)、生殖能力が記録された優先事項である女性が含まれる。これは万能な医学ではない。個々の生殖タイムラインとがん治療の緊急性を尊重する精密医学だ。
初期試験データはこのアプローチを検証する。骨盤放射線前に転位を受けた女性は、未治療対照群と比較して60–80%高い率で卵巣機能を保持した。寛解後の妊娠率は小規模コホートで40–60%の範囲であり、より大規模な前向き研究が現在主要がんセンター全体で進行中である。技術的改善(血管完全性の維持、癒着の防止、再配置幾何学の最適化)は継続的に転帰を改善している。
- 隣接する機会*:外科技術が成熟するにつれて、生殖能力統合腫瘍学の出現を目撃している。生殖能力保存が事後的に接ぎ木されるのではなく、初期治療計画に組み込まれる新しい専門分野。これは以下のための空白を開く:(1)最高確率の候補者を特定するためのAI駆動患者マッチング;(2)臓器再配置を最適化するためのリアルタイム外科シミュレーション;(3)生存者を数十年にわたって追跡する縦断的生殖能力追跡プラットフォーム;(4)生殖能力保存を選択的追加ではなく予防的ケアとして認識する保険モデル。
術後モニタリングは臓器配置の超音波検証とホルモン評価(AMH、FSH、エストラジオール)を含み、機能的保存を確認する。患者は通常、がん寛解が確認されるまで妊娠試行を延期する。通常、がんの種類、ステージ、予後に応じて治療後6–12ヶ月。この待機期間自体が価値を持つようになる。心理的調整、関係の安定化、家族計画のタイミングについての情報に基づいた意思決定を可能にする。
- 長期的ビジョン*:すべてのがんセンターが生殖の未来オフィスを運営する未来を想像せよ。新たに診断された患者と面会し、生殖能力保存選択肢をマッピングし、外科的タイミングを調整し、寛解を通じてケアの継続性を維持する専任チーム。このインフラ転換は生殖能力を反応的介入から積極的人生建築に変える。
生殖健康に対する放射線と化学療法の影響の管理:損傷軽減から再生医学へ
放射線と化学療法は十分に理解されたメカニズムを通じて生殖損傷を与える。卵母細胞のDNA二本鎖切断、原始卵胞プールの枯渇、卵子の質の低下。しかし本質的な問題は〜にあるのではなく、この課題の中に生殖能力を保護し回復する方法を根本的に再想像する深刻な機会が存在することにある。
放射線感受性は用量によって予測可能に変動する。一時的不妊は6–8 Gray(Gy)付近で出現;永続的不妊は通常20 Gy以上で生じる。化学療法薬剤、特にアルキル化薬(シクロホスファミド)と白金化合物は、生殖細胞毒性を通じて卵巣予備能を直接損なう。これらの用量反応関係を理解することで、精密遮蔽と防御的介入が可能になる。
-
予見としての評価*:治療前生殖能力評価は標準的腫瘍学的実践となるべきだ。抗ミュラー管ホルモン(AMH)検査は卵巣予備能を定量化;経膣超音波は前胞状卵胞を計数;エストラジオールとFSHパネルはホルモン基礎値を確立する。これらのメトリクスは現在の状態を記録するだけでなく、治療後の回復軌跡を予測し、妊娠タイミング戦略を指導する。35歳未満の若年患者は通常1–2年以内に卵巣機能を回復;40歳以上の患者はより急峻な生殖能力低下に直面し、保存決定をより緊急にする。
-
リアルタイムでの防御的革新*:化学療法中のゴナドトロピン放出ホルモンアゴニスト(GnRH-a)を用いた卵巣抑制は、新興研究で損傷を20–30%低減する。意味のあるが控えめなバッファ。放射線照射野の最適化は、臨床的に実行可能な場合、がん転帰を損なわずに生殖器官を遮蔽する。これらは競合する優先事項ではない。統一された治療アーキテクチャ内の補完的戦略だ。
生殖能力保存メニューは劇的に拡大した。卵子凍結(卵母細胞凍結保存)は柔軟性を提供する。患者は寛解後数年で時間的プレッシャーなしに妊娠を追求できる。胚凍結保存はパートナーを持つ者にとってより高い成功率を提供する。卵巣組織凍結保存は最前線を表す。凍結組織は寛解後に再移植でき、生殖能力と内分泌機能の両方を潜在的に回復させる。しかしタイミングは依然として重要だ。卵子採取は10–14日を要し、がん治療を転帰を損なわずに遅延させることができる場合にのみ実行可能。
-
再生的地平*:保存を超えて、生殖能力回復の時代に入りつつある。新興研究は卵巣組織を再生するための幹細胞療法、体外配偶子形成(幹細胞から卵子を作成)、治療後生殖能力を最適化するための個別化ホルモンプロトコルを探索している。これらは遠い可能性ではない。現在臨床試験中だ。5–10年以内に、がん生存者は単に生殖能力を回復するだけでなく、完全な生殖的自律性を回復させる再生選択肢にアクセスできるかもしれない。
-
知識労働者と意思決定者のための実行可能な含意*:がんケアを管理する組織は生殖能力保存を非交渉的標準として確立すべきだ。これは以下を意味する:(1)腫瘍学的摂取に組み込まれた生殖専門医との治療前相談;(2)治療計画に記録された文書化された患者選好;(3)がん緊急性と生殖能力タイムラインの両方に対応する外科および保存手順のスケジューリング;(4)数十年にわたって生殖健康を監視する縦断的追跡システム;(5)生殖能力保存を裁量的支出ではなく予防的医学として扱う保険適用。
より深い洞察:生殖能力を生殖能力保存の周辺ではなく中核的健康転帰として扱うことは、治療成功をいかに測定するかを根本的に再構成する。生存率は重要だ。生存者がその後に構築する人生も同様に重要だ。