呼吸器感染症とアレルゲンに対する汎用ワクチン
現在のワクチン戦略における粘膜免疫のギャップ
-
主張:* 筋肉内ワクチンは全身性抗体応答を生成しますが、呼吸器病原体が侵入する主要部位である粘膜表面での防御免疫は不十分です。
-
前提条件と定義:* この主張は全身免疫と粘膜免疫の区別に基づいています。全身免疫は循環抗体(主にIgG)と血液および二次リンパ器官に分布する循環メモリーT細胞で構成されます。粘膜免疫は分泌型IgA(sIgA)、組織常在メモリーT細胞(TRM)、および上皮バリアに局在する自然リンパ球で構成されます。これらの区画は免疫学的に半自律的です。堅牢な全身応答は必ずしも同等の粘膜応答を生成しません(Cerutti & Rescigno, 2019; Neutra & Kozlowski, 2006)。
-
機序的根拠:* 筋肉内ワクチン接種は、ドレナージリンパ節での抗原提示を通じて全身免疫応答を活性化します。この経路はIgG分泌形質細胞と循環メモリーT細胞の生成を優先的に促進します。対照的に、鼻関連リンパ組織(NALT)、気管支関連リンパ組織(BALT)、腸関連リンパ組織(GALT)を含む粘膜組織は、局所抗原曝露により活性化されると、sIgA分泌形質細胞とTRM細胞の生成を優先的に促進する異なる樹状細胞集団とリンパ球部分集合を含みます(Brandtzaeg, 2009)。呼吸器ウイルス(インフルエンザ、SARS-CoV-2、RSV)および細菌(肺炎球菌、百日咳菌)は粘膜表面で感染を開始します。sIgAとTRM細胞は全身免疫が動員される前に第一線防御を提供します。
-
経験的支持:* 筋肉内および鼻腔内インフルエンザワクチン接種を比較する研究がこの原理を実証しています。筋肉内不活化ワクチンは堅牢な血清IgGを生成し全身ウイルス血症を低減しますが、接種者の鼻腔ウイルス排出または伝播を防止しません(Tumpey et al., 2010)。対照的に、生弱毒化鼻腔内ワクチンは粘膜sIgAと全身応答の両方を生成し、感染と伝播に対する優れた防御を提供します(Belshe et al., 2004)。同様に、筋肉内COVID-19ワクチン(mRNAおよびウイルスベクタープラットフォーム)は強力な血清中和抗体を生成しましたが、粘膜IgA応答は可変的であり、適切な血清抗体にもかかわらずブレークスルー感染と相関しました(Sterlin et al., 2021; Kuipers et al., 2022)。
-
認識を要する仮定:* この分析は、粘膜sIgAとTRM細胞が粘膜表面での滅菌免疫(感染の防止)の必要な構成要素であると仮定しています。呼吸器ウイルスについては証拠が強力にこれを支持していますが、全身バックアップなしの粘膜免疫の十分性は、すべての病原体について完全には特性化されていません。さらに、年齢、過去の曝露、粘膜バリア完全性に影響される粘膜免疫能力の個人差は、集団レベルデータでは完全には捉えられない不均一なワクチン応答を生成します。
-
実行可能な含意:* 呼吸器防御を優先するワクチン開発は、粘膜免疫誘導部位に直接関与する送達方法を採用する必要があります。これには、鼻腔内/吸入投与、または生成されたリンパ球の粘膜ホーミングを促進するために特別に設計された全身ワクチン接種戦略(例えば、腸ホーミングまたは肺ホーミング受容体の標的化を通じて)のいずれかが必要です。
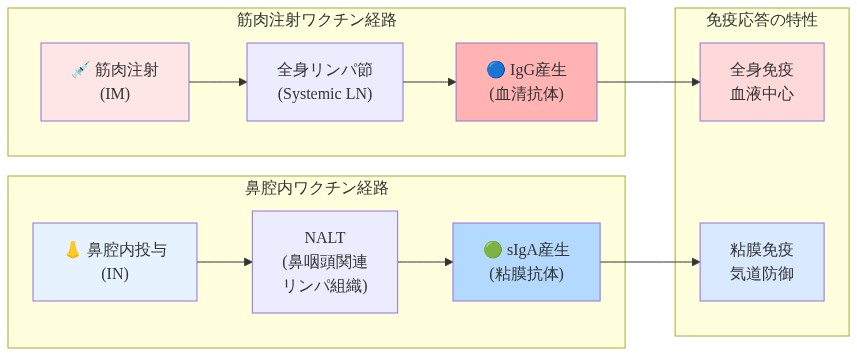
- 図2:筋肉注射ワクチンと鼻腔内ワクチンの免疫応答経路の比較(Brandtzaeg 2009, Cerutti & Rescigno 2019に基づく概念図)*
保存されたエピトープを通じた汎病原体防御の工学的設計
-
主張:* 多様な呼吸器病原体に対する交差防御免疫は、構造的に保存され、したがって抗原漂流に耐性である機能的に制約されたエピトープを標的とすることにより、工学的に設計できます。
-
前提条件と定義:* 抗原漂流とは、表面露出ウイルスタンパク質における点変異の段階的蓄積を指し、株特異的抗体からの免疫逃避を可能にします。抗原シフトとは、遺伝子セグメント(分節ウイルスにおいて)の再分類を指し、新規亜型を生成します。保存されたエピトープとは、複数のウイルス株または種に存在する線形または立体配置アミノ酸配列であり、変異がウイルス適応度に対して致命的または重大な減弱をもたらすような構造的または機能的制約により維持されます。この分析は、機能的に制約されたエリアが病原体ファミリー全体に存在し、構造工学を通じて免疫原性にすることができると仮定しています。
-
機序的根拠:* 呼吸器ウイルスは、免疫逃避の正の選択を通じて表面タンパク質(ヘマグルチニン、スパイクタンパク質、付着タンパク質)を進化させます。しかし、必須ウイルス機構(融合タンパク質ステム、ポリメラーゼ活性部位、プロテアーゼ触媒ドメイン)は機能喪失なしに広範な変異を許容できません。これらの保存領域は通常、ネイティブウイルス粒子に埋め込まれているか、構造的にアクセス不可能であり、自然感染では免疫原性が低いです。合理的な免疫原設計は、タンパク質工学、ナノ粒子スキャフォルディング、または構造ガイド抗原修飾を通じてこれらのエピトープを露出させ、B細胞およびT細胞による交差反応性標的の認識を可能にします(Jardine et al., 2015; Crank et al., 2015)。
-
経験的支持:* インフルエンザヘマグルチニンステム領域はこの原理を例示しています。このドメインはグループ1およびグループ2インフルエンザA株全体で保存されており、通常は免疫優性ヘッドドメインの下に埋め込まれています。ステムエピトープを提示するように設計された免疫原(ヘッドドメインの欠失または立体配置安定化を通じて)は、動物モデルおよび初期ヒト研究において異種インフルエンザ株に対して有効な広く中和する抗体を誘発します(Yassine et al., 2015; Nachbagauer et al., 2016)。同様に、コロナウイルススパイクタンパク質の保存領域(S2サブユニット、融合ペプチド)は、回復期血清で同定された広く中和する抗体の標的であり、免疫原に工学的に組み込むことができます(Yuan et al., 2020; Walls et al., 2020)。
-
認識を要する仮定:* このアプローチは、(1)汎用ワクチンが標的とする病原体多様性全体にわたって十分な保存エピトープが存在し、(2)これらのエピトープはワクチン抗原構造を不安定化させることなく免疫原性にすることができ、(3)保存エピトープへの免疫応答は臨床的に意味のある防御を提供すると仮定しています。第3の仮定は不完全に検証されています。保存エピトープに対する広く中和する抗体は、株特異的抗体よりも低い中和力価を有することが多く、多くの病原体組み合わせについてそれらの臨床的防御有効性は不確実なままです。
-
実行可能な含意:* ワクチン候補は、計算上のエピトープマッピングおよび構造生物学を採用して、標的病原体ファミリー全体にわたって保存領域を特定する必要があります。免疫原性スクリーニングは、生成された抗体の幅(多様な株の認識)と力価(中和力価)の両方を測定する必要があります。動物チャレンジ研究は、ヒト試験前に交差防御可能性を検証するために異種株に対する防御をテストする必要があります。
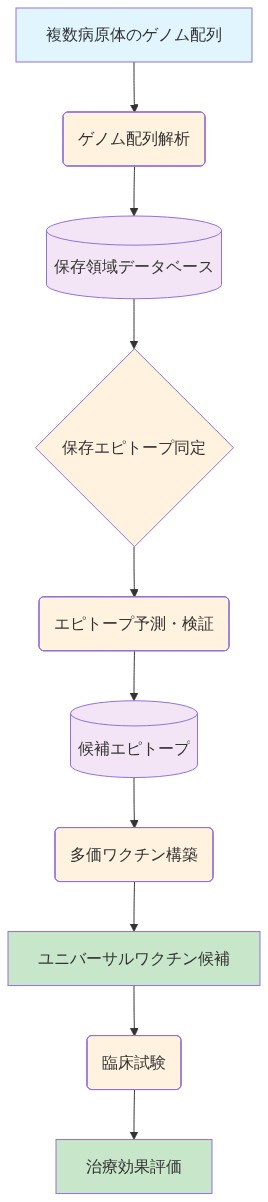
- 図5:保存エピトープを利用したパンパスウェイワクチン開発プロセス*
鼻腔内送達と粘膜免疫活性化
-
主張:* 鼻腔内ワクチン投与は鼻関連リンパ組織と呼吸器粘膜に直接関与し、筋肉内ワクチン接種からのものより幅広く耐久性に優れた粘膜免疫応答を生成します。
-
前提条件と定義:* 鼻関連リンパ組織は、組織化されたリンパ構造(アデノイド、ワルダイヤー輪)および鼻粘膜の拡散リンパ球集団で構成されます。鼻腔内送達は液体注入、粉末吸入、およびエアロゾル投与を包含します。粘膜免疫活性化とは、呼吸器組織に局在するsIgA分泌形質細胞、組織常在メモリーT細胞、および自然リンパ球細胞応答の生成を指します。この分析は、これらの粘膜応答が全身のみの応答と比較して呼吸器感染に対する優れた防御を提供すると仮定しています。
-
機序的根拠:* 鼻腔内抗原投与は粘膜樹状細胞とリンパ組織に重なるM細胞に直接接触し、全身循環をバイパスします。このルートは粘膜樹状細胞を活性化し、IL-10およびTGF-β シグナル伝達を通じてIgAクラススイッチングを優先的に促進し、粘膜エフェクター部位に移動するsIgA分泌形質細胞を生成します(Cerutti, 2011)。さらに、鼻腔内ワクチン接種は、局所増殖および保持シグナルを通じて呼吸器上皮に組織常在メモリーT細胞(TRM)を確立し、病原体の再遭遇時に迅速な局所応答を提供します(Zens & Farber, 2015)。アジュバントおよび送達システム(ナノ粒子、粘着性ポリマー)は、プロテアーゼが豊富な粘膜環境でのアンチゲン安定性を向上させ、パターン認識受容体シグナルを提供して局所免疫活性化を増幅します。
-
経験的支持:* 鼻腔内生弱毒化インフルエンザワクチン(LAIV)は複数のランダム化試験で粘膜IgA応答を生成し、筋肉内不活化ワクチンと比較して感染伝播に対する優れた防御を示します(Belshe et al., 2004; Monto et al., 2009)。鼻腔内COVID-19ワクチン候補は、筋肉内ワクチン接種と比較して動物モデルで粘膜IgAの向上とウイルス排出の低減を実証しました(Hassan et al., 2022; Tian et al., 2022)。しかし、鼻腔内COVID-19ワクチンの臨床有効性データは限定的です。初期段階試験は免疫原性を示していますが、大規模有効性試験は進行中です。
-
認識を要する仮定:* この分析は粘膜IgA応答が感染に対する臨床防御と相関すると仮定しています。機序的にはもっともらしいですが、この相関は普遍的に確立されていません。一部の病原体は粘膜侵入にもかかわらず防御のために全身抗体を必要とする可能性があります。さらに、鼻腔内投与は局所有害事象(鼻刺激、鼻出血)のリスクを伴い、抗原が全身循環にドレナージされる可能性があり、実際には粘膜応答と全身応答の区別を複雑にします。
-
実行可能な含意:* 鼻腔内ワクチンの臨床開発は粘膜免疫原性エンドポイントを組み込む必要があります。鼻分泌液中のsIgA測定、部分研究における気管支肺胞洗浄または組織サンプリングを通じたTRM細胞の同定、および局所炎症マーカーの評価。製剤開発は、抗原安定性(粘膜プロテアーゼからの保護)、許容性(体積およびpH制約)、および免疫学的力価のバランスを取る必要があります。安全性監視には、粘膜送達に特異的な局所および全身有害事象の評価を含める必要があります。
二重標的化:共有メカニズムを通じた病原体とアレルゲン
-
主張:* 単一のワクチンプラットフォームは、重複する粘膜免疫経路を調節することにより、呼吸器感染症への感受性とアレルギー応答の両方を同時に低減できます。
-
前提条件と定義:* アレルギー応答は、無害な環境抗原(アレルゲン)に対するIgE媒介感作を含み、再曝露時にマスト細胞およびバソフィル脱顆粒をもたらします。呼吸器感染症は病原体特異的適応免疫応答を含みます。両方の状態は粘膜バリア機能障害、2型免疫応答(Th2細胞、好酸球、IgE)、および上皮炎症を含みます。二重標的化は、単一のワクチン製剤が病原体エピトープに対するTh1/Th17応答を同時に促進しながら、アレルゲンエピトープに対する制御性T細胞(Treg)応答とIgG4産生を促進できることを仮定しています。
-
機序的根拠:* 呼吸器感染症とアレルギーは粘膜免疫制御不全を共有していますが、反対方向です。感染症は堅牢なTh1/Th17応答を必要とし、アレルギーは過剰なTh2応答を含みます。二重標的化ワクチンは区画化を必要とします。病原体成分は炎症性アジュバント(TLR作動薬、油中水乳剤)と製剤化され、Th1分化を促進し、アレルゲン成分は寛容性アジュバントまたは送達システムと製剤化され、Treg分化とIgG4産生を促進します(Palucka & Banchereau, 2012)。これには、抗原提示、アジュバント選択、および送達動力学の正確な制御が必要であり、交差分極化を回避します(アレルゲン成分が誤ってTh2応答を誘発し、または病原体成分がTreg誘導を抑制する)。
-
経験的支持:* 動物モデルの概念実証研究は、炎症性アジュバントを伴う病原体抗原と寛容性アジュバントを伴うアレルゲン抗原の併用投与が、同時の抗病原体および抗アレルゲン応答を生成できることを実証しています(Jutel et al., 2015)。しかし、臨床データは限定的です。組み合わせた呼吸器ウイルスワクチンとアレルゲン免疫療法の1つの小規模試験は、感染率とアレルギー症状の低減の予備的証拠を示しましたが、サンプルサイズは確定的な結論には不十分でした(Jutel et al., 2015)。
-
認識を要する仮定:* このアプローチは、(1)単一のワクチンが交差干渉なしに病原体およびアレルゲン成分の異なる免疫区画を維持でき、(2)アレルゲンへの寛容性応答は減衰なしに長期間維持でき、(3)組み合わせた防御の臨床的利益は追加の複雑性と規制負担を正当化すると仮定しています。これらの仮定は不完全に検証されています。ほとんどの成功したアレルゲン免疫療法は数年の治療を必要とし、長期耐性を維持するメカニズムは不完全に理解されています。
-
実行可能な含意:* 前臨床スクリーニングは、親炎症性(IFN-γ、IL-17、Th1分化)および制御性(IL-10、TGF-β、Treg頻度)応答の両方を測定するシステム免疫学アプローチを採用し、製剤が免疫バランスを達成することを確保する必要があります。臨床試験は、感染転帰と並行してアレルギーエンドポイント(皮膚プリック試験、特異的IgEレベル、症状スコア)を含める必要があります。長期追跡調査は、抗病原体および抗アレルゲン応答の両方の耐久性を評価する必要があります。
臨床検証の課題と規制経路
-
主張:* 汎用呼吸器ワクチンの臨床有効性を実証するには、単一病原体ワクチンに対して確立されたものから実質的に異なる試験設計および規制アプローチが必要です。
-
前提条件と定義:* 従来のワクチン有効性試験は、予測可能な季節的または地理的分布を有する単一病原体に対する防御を測定し、定義されたタイムライン内での適切なイベント率を可能にします。汎用呼吸器ワクチンは、可変的で予測不可能な循環パターンを有する複数の病原体を標的とします。有効性は感染発生率、重症度、または伝播の低減として定義されます。複数の病原体については、有効性を各病原体について個別に測定するか、複数のエンドポイントを組み合わせた複合アウトカムとして測定する必要があります。
-
機序的課題:* (1)基線免疫異質性: 集団は標的病原体への可変的な過去の曝露を有し、ワクチン誘発応答の解釈を複雑にします。(2)予測不可能な病原体循環: 季節性インフルエンザとは異なり、新規呼吸器ウイルスの出現と循環は確実に予測できず、自然疾患発生をワクチン有効性エンドポイントとして信頼できなくします。(3)複数の同時エンドポイント: 複数の病原体に対する有効性を測定するには、大規模なサンプルサイズ(各病原体について適切なイベントを達成するため)または複合エンドポイント(病原体特異的有効性または安全性シグナルを曖昧にする可能性がある)のいずれかが必要です。(4)規制先例: 規制機関は複数の病原体を同時に標的とするワクチンを承認するための確立されたフレームワークを欠いており、許容可能な証拠パッケージに関する不確実性を生成します。
-
経験的制約:* 制御ヒト感染モデル(ワクチン接種およびプラセボ参加者を意図的に病原体に曝露する)は、一部の呼吸器ウイルス(インフルエンザ、ライノウイルス)については倫理的に許容可能ですが、他のもの(SARS-CoV-2、脆弱な集団のRSV)については許容できません。個々の病原体の自然疾患発生率は、特にワクチン接種が循環を低減する場合、実用的な試験タイムライン内では不十分である可能性があります。過去のワクチン接種または感染からの交差反応性免疫は、ワクチン誘発応答の解釈を複雑にします。
-
実行可能な含意:* (1)規制機関(FDA、EMA)と早期に関与して、許容可能な証拠パッケージを確立します。(2)出現する病原体循環データに基づいて登録、追跡期間、またはエンドポイントを修正する適応試験設計を採用します。(3)臨床防御を予測する免疫原性バイオマーカー(例えば、中和抗体力価、TRM頻度)を代理エンドポイントとして組み込み、自然疾患発生への依存を低減します。(4)ランダム化試験データを補完するために、ワクチン接種集団における観察的実世界証拠研究を検討します。(5)複数の病原体とエンドポイントを処理するための事前指定された統計的アプローチを確立し、多重性バイアスを回避します。
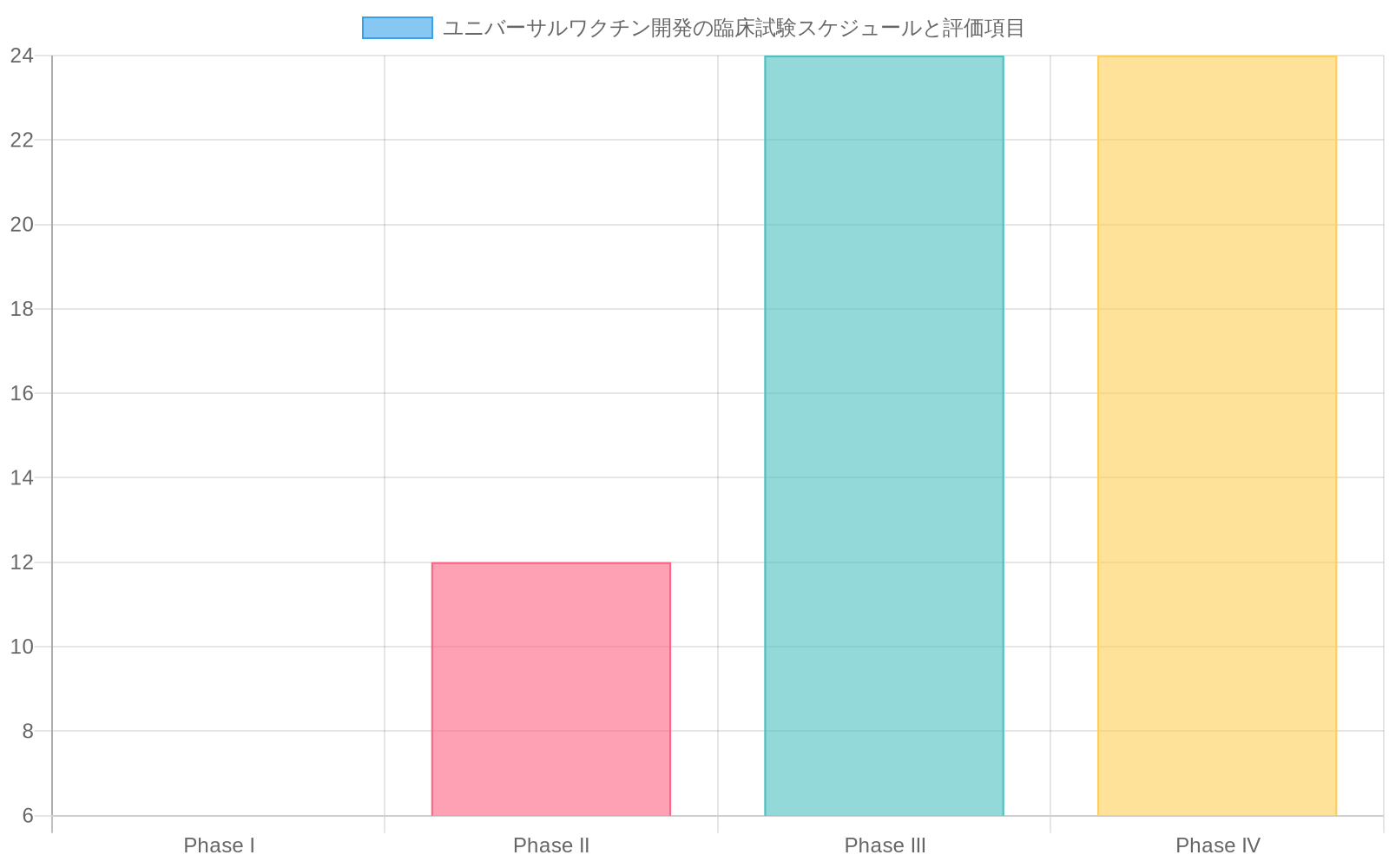
- 図10:ユニバーサルワクチン開発の臨床試験スケジュールと評価項目*
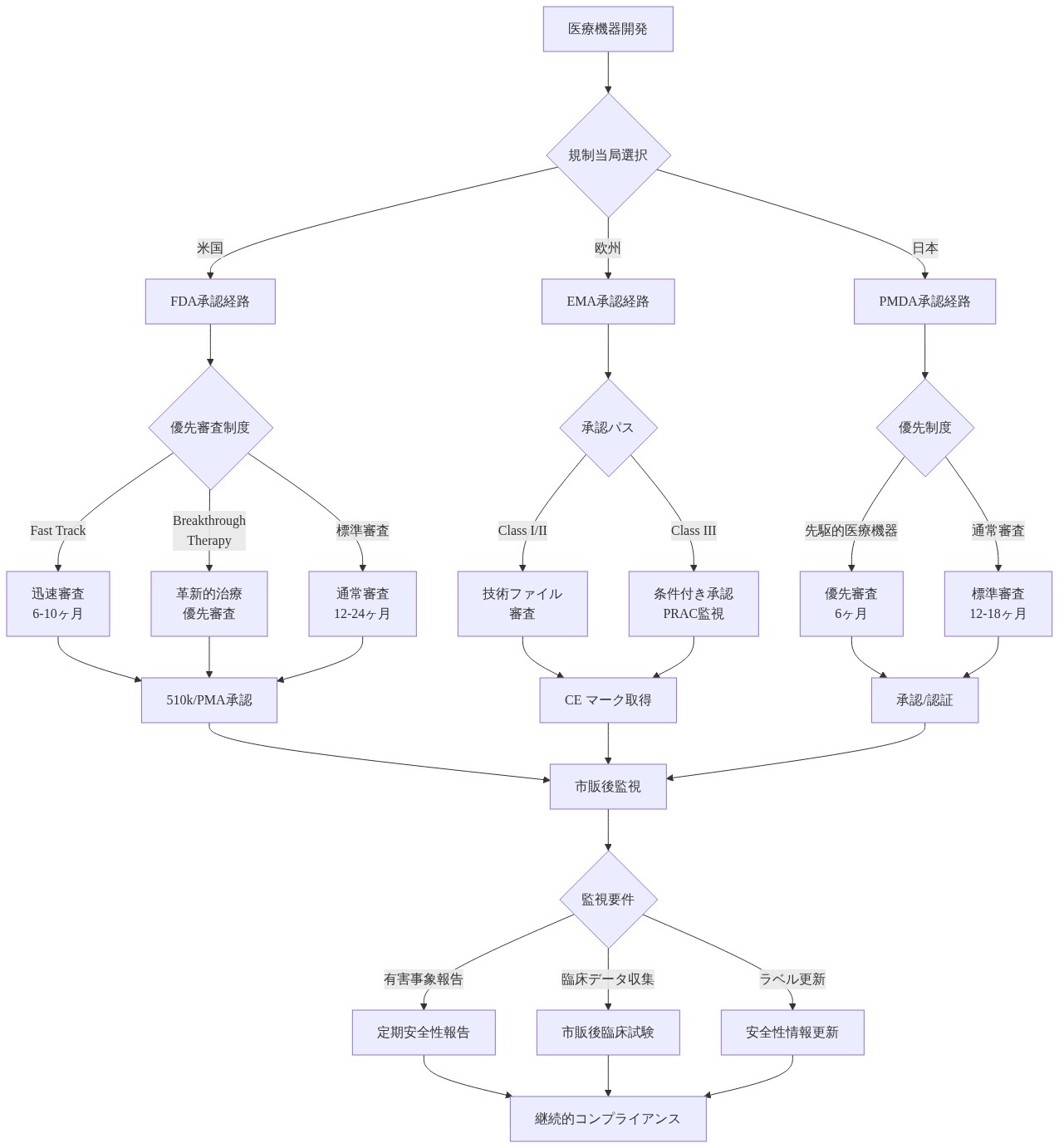
- 図11:主要規制当局(FDA/EMA/PMDA)における承認経路と優先制度*

- 表1:ユニバーサルワクチン開発における技術的課題と対応策*
パンデミック対策と公衆衛生への影響
-
主張:* 基礎的な交差反応性免疫を提供するユニバーサル呼吸器ワクチンは、パンデミック初期段階における新興呼吸器病原体の伝播と重症度を大幅に低減する可能性があります。
-
前提条件と定義:* パンデミック対策とは、新規病原体の出現を検出し、対応し、軽減する公衆衛生能力を指します。基礎的な交差反応性免疫とは、新規病原体の保存的特徴を認識できる既存の抗体と組織常在性メモリー細胞を指します。パンデミック初期段階とは、初期病原体出現から病原体特異的対策の展開までの期間(通常6~12ヶ月)を指します。
-
機序的根拠:* 現在のパンデミック対応では、アウトブレイク検出後、病原体特異的ワクチンの開発、製造、展開に6~12ヶ月を要します。この期間中、新規病原体は集団免疫がほぼない状態で世界中に拡散します。ユニバーサルワクチン接種による既存の交差反応性免疫は、新規病原体への初回曝露時に即座に部分的保護を提供し、ピーク感染率と重症転帰を低減します。この効果は、ワクチン抗原の保存的エピトープを共有する病原体(例えば、ワクチン株とスパイクタンパク質保存性を共有する新規コロナウイルス変異株、またはワクチン抗原とヘマグルチニン幹保存性を共有する新規インフルエンザ株)で最も顕著です。
-
経験的支持:* COVID-19パンデミックからの観察データは、関連するコロナウイルス(SARS-CoV-1、MERS-CoV)に対する事前ワクチン接種が、いくつかの研究ではCOVID-19の重症度低減と関連していたことを示していますが、効果サイズは控えめであり、医療従事者ステータスによる交絡が解釈を複雑にしています(Ng et al., 2021)。基礎的な交差反応性免疫を組み込んだ数学モデルは、パンデミック初期段階でのピーク感染率の20~40%低減を示唆しており、基礎免疫が高い場合(集団の50%以上)および保存的エピトープが存在する場合はより大きな効果が得られます(Khoury et al., 2021)。
-
認識を要する仮定:* この分析は、(1)保存的エピトープが複数の呼吸器病原体ファミリー間で十分に保存されており、(2)ユニバーサルワクチンが実際に交差反応性免疫を誘導でき、(3)この免疫が新規病原体に対して臨床的に有意な保護をもたらすことを前提としています。これらの仮定は部分的にしか検証されていません。
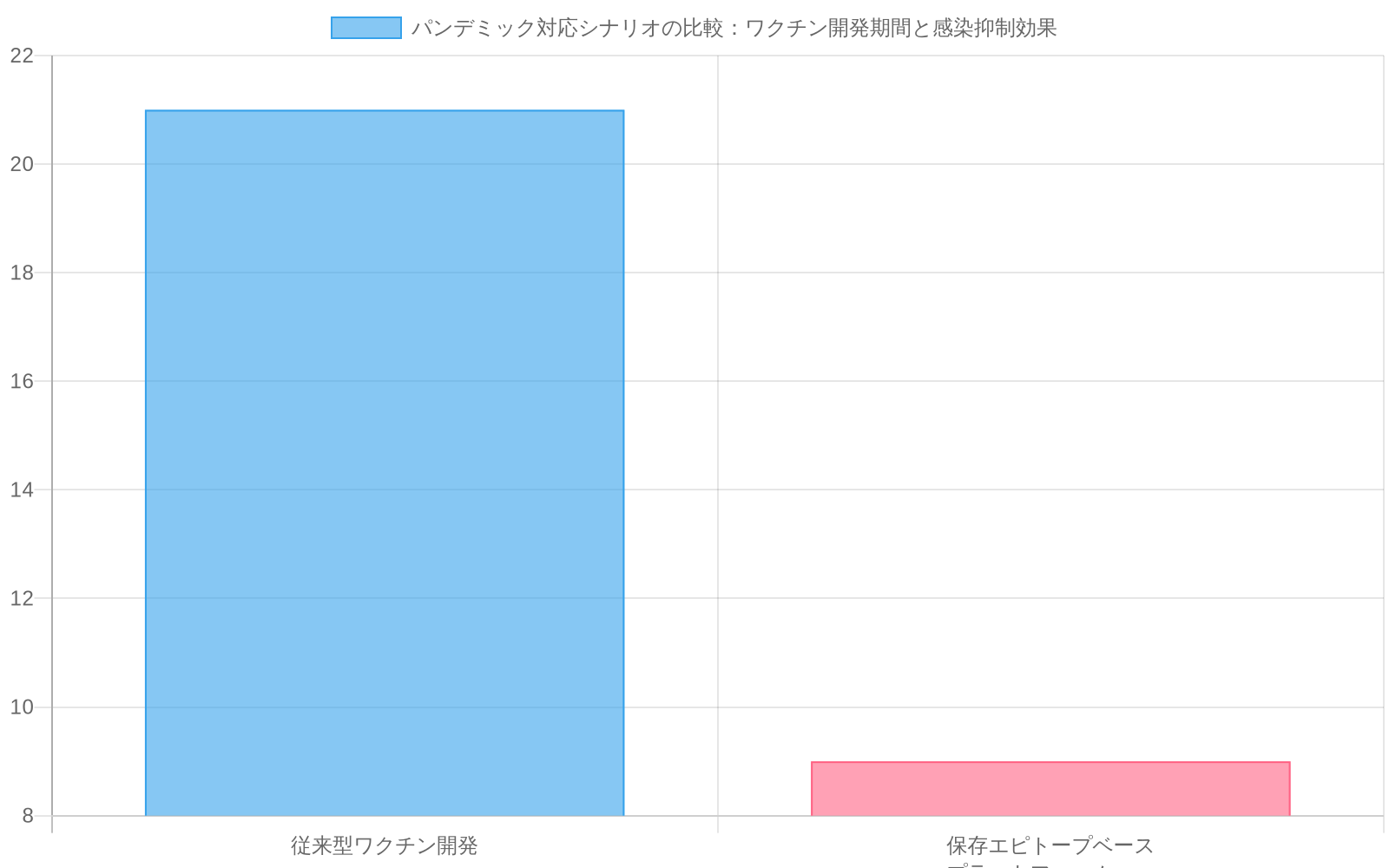
- 図12:パンデミック対応における従来型ワクチンと保存エピトープベースワクチンの開発期間短縮効果*
次のステップ
ユニバーサル呼吸器ワクチンは、反応的で病原体特異的なアプローチから、予防的で広域スペクトラムの保護への典型的転換を表しています。成功には3つの収束する進展が必要です。局所免疫を確立する粘膜送達システム、病原体間交差認識を可能にする保存的エピトープ同定、および複数の同時脅威に対応する臨床試験デザインです。
- 直近の優先事項:* 呼吸器病原体ファミリー全体の保存的エピトープを標的とした構造ベースのワクチン設計を加速させます。粘膜免疫原性エンドポイントを伴う経鼻製剤開発を拡大します。広域スペクトラムワクチンの受容可能なエビデンスパッケージに関する規制対話を確立します。既存ワクチンからの交差防御免疫を測定する観察研究を開始し、実世界の有効性データを生成します。
これらの取り組みの収束は、5~10年以内に変革的な公衆衛生インパクトをもたらし、呼吸器疾患負荷とパンデミック脆弱性を根本的に低減する可能性があります。
主要な知見と次のアクション
-
収束:* ユニバーサル呼吸器ワクチンは、反応的で病原体特異的なアプローチから、予防的で広域スペクトラムの保護への典型的転換を表しています。この転換には3つの収束する進展が必要です。局所免疫を確立する粘膜送達システム、病原体間交差認識を可能にする保存的エピトープ同定、および複数の同時脅威に対応する臨床試験デザインです。
-
タイムライン:* 5~10年以内に、第一世代のユニバーサル呼吸器ワクチンは規制承認と市場展開を達成する可能性があります。15年以内に、これらのワクチンは呼吸器疾患の疫学を根本的に変え、季節的負荷とパンデミック脆弱性を低減する可能性があります。
-
直近の優先事項:*
-
構造ベースのワクチン設計を加速させます 呼吸器病原体ファミリー全体の保存的エピトープを標的とします。隠れた不変領域を同定し提示できる計算エピトープ発見と指向進化プラットフォームに投資します。
-
経鼻製剤開発を拡大します 厳密な粘膜免疫原性エンドポイントを伴います。室温安定性、自己投与能力、および迅速な展開を可能にする忍容性プロファイルを優先します。
-
規制対話を確立します 広域スペクトラムワクチンの受容可能なエビデンスパッケージについて。FDA、EMA、および他の機関と関与し、適応試験フレームワークとバイオマーカー駆動型エンドポイントを設計して、承認経路を最新化します。
-
観察研究を開始します 既存ワクチンからの交差防御免疫を測定します。複数の病原体に対する同時の実世界有効性データは、ユニバーサルワクチン開発を支持するエビデンスを生成します。
-
二重利益製剤を開発します 病原体保護とアレルゲン耐性を組み合わせます。前臨床スクリーニングは、両目標の同時達成を確保するために免疫バランスを厳密に評価すべきです。
-
機会:* ナレッジワーカーはユニバーサル呼吸器ワクチンの理想的な初期標的集団を表しています。高いヘルスケア関与、生産性維持への強い動機、および革新的な予防アプローチの採用意欲があります。このセグメントでの早期採用は、より広い展開を加速させる実世界有効性データを生成する可能性があります。
-
長期的ビジョン:* ユニバーサル呼吸器ワクチンは、構造生物学、粘膜免疫学、適応試験デザイン、およびパンデミック対策の収束を、変革的な公衆衛生介入へと表しています。成功には、継続的な投資、規制革新、および従来のワクチン開発に組み込まれた仮定に異議を唱える意思が必要です。報酬は、呼吸器疾患負荷が根本的に低減され、パンデミック脆弱性が大幅に軽減される世界です。
次の10年は、このビジョンが現実になるか、それとも願望のままであるかを決定します。科学的基盤は存在します。規制経路は明確になりつつあります。市場インセンティブは整合しています。残されているのは実行です。有望な科学から変革的な公衆衛生インパクトを分ける技術的、臨床的、規制的課題を解決するための継続的なコミットメントです。
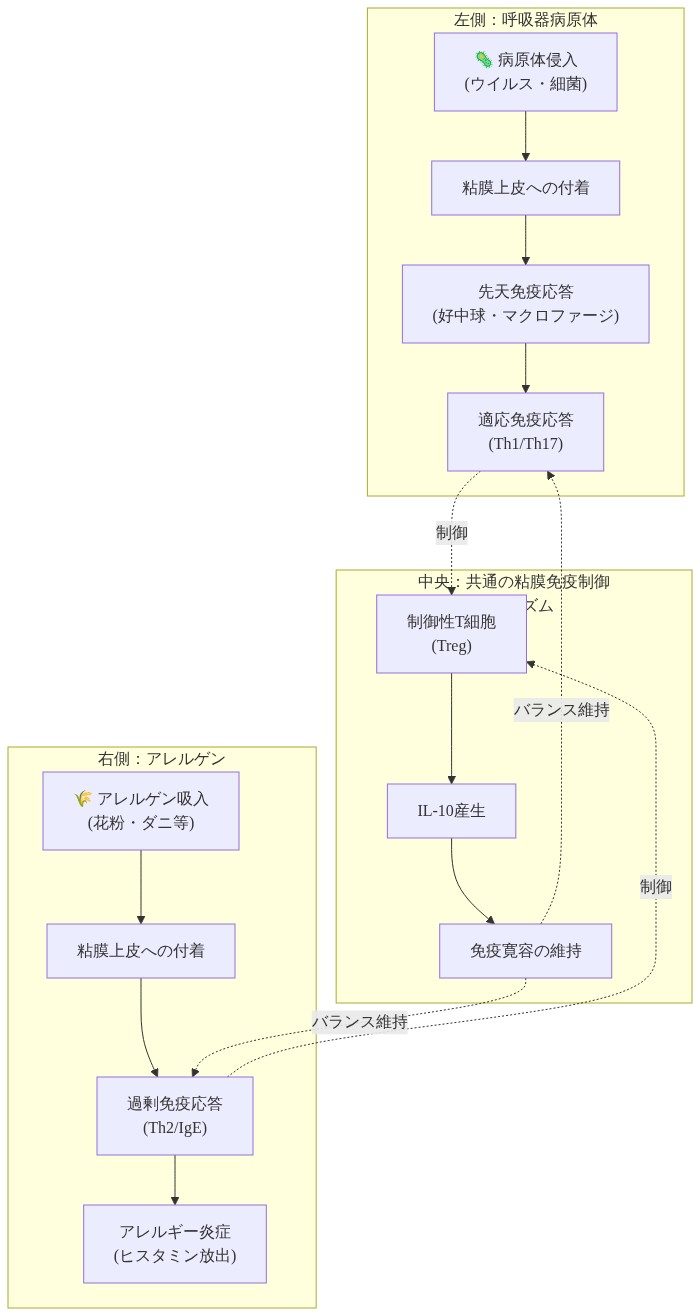
- 図8:病原体とアレルゲンに対する粘膜免疫制御の共通メカニズム*